Nyretransplantation: En gennemgang af robotassisteret nyretransplantation
Mar 18, 2022
Kontakt:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Levende donor Robot-assisteret nyretransplantation: en ny standard for pleje?
Andrea Gallipoli. Juan Gomez Rivas. Alessandro Larcher. Alberto Breda
Abstrakt
Formål med anmeldelseRobot-assisteret nyretransplantation(RAKT) har potentialet til at kombinere fordelene ved minimalt invasiv kirurgi med den bedste nyreerstatningsbehandling. I løbet af det sidste årti var resultaterne opmuntrende, da kirurgiske og funktionelle resultater synes optimale i levende donation. Nylige undersøgelser fokuserede på sammenligningen med åbennyretransplantation(OKT), særlige situationer såsom overvægtige patienter eller transplantationer af flere kar og optimering af teknikken for at øge dens kirurgiske indikationer.
Seneste fund i forhold til OKT, RAKT(Robot-assisteret nyretransplantation) har en længere genopvarmningstid og operationstid, men lavere intraoperativt blodtab. Sårrelaterede hændelser og postoperative smerter falder med robotteknik. Dette er også blevet påvist hos overvægtige patienter, hvor RAKT(Robot-assisteret nyretransplantation)kan være særlig gavnlig. Der blev ikke fundet nogen signifikant forskel i graftfunktion, graftoverlevelse og patientoverlevelse med RAKT(Robot-assisteret nyretransplantation)og OKT i kort- og mellemtidsopfølgning. Et transplantat med flere kar bør ikke betragtes som en kontraindikation til robotkirurgi. Intrakorporale kølesystemer til regional hypotermi er ikke blevet anvendt i RAKT(Robot-assisteret nyretransplantation)endnu. Fremtidige udfordringer vil være inklusion af patienter med ateromatøse iliaca arterier og transplantationsprogrammer for afdøde donorer. Sammenfatning Et randomiseret-kontrolleret forsøg er nødvendigt for endeligt at bekræfte resultaterne af retrospektive og prospektive kohortestudier. Implementeringen af proceduren i flere centre afhænger af bredere indikationer, hvilket i sidste ende kan reducere procedurerelaterede omkostninger. For at garantere anvendeligheden af RAKT(Robot-assisteret nyretransplantation)fra afdøde donorer er det fundamentalt at optimere transplantatets kølesystemer og at inkludere modtagere med ateromatøse iliaca arterier.
Nøgleord: Nyretransplantation· Regional hypotermi ·Robot-assisteret nyretransplantation· Robotkirurgi · Vaskulær anastomose

cistanche mandlige fordele
Introduktion
Åbennyretransplantation(OKT) betragtes som standarden for pleje i nyreerstatningsbehandling[1]. I anden halvdel af forrige århundrede var virkningen af denne kirurgiske teknik dramatisk. I 1950 udførte Richard Lawler det første orto-emnenyretransplantation, mens RenéKüss i 1952 dirigerede den første ekstraperitonealenyretransplantationmed iliac kar anastomoser og ureteroneocystostomi. Begge procedurer viste en indledende graftfunktion med en hurtig forringelse af nyren. Den første vellykkede kadavernyretransplantation(1953) fik Nobelprisen i medicin 1990 til Joseph Murray, som forfinede René Küss' teknik. Det skal bemærkes, at sidstnævnte forbliver den eneste Nobelpris, der er tildelt for kirurgisk behandling i de sidste 70 år. En anden stor kirurgisk innovation er udviklingen af minimalt invasiv kirurgi, som hurtigt omformede urologisk kirurgi i løbet af de sidste 30 år. Implementeringen af mindre instrumenter fører til mindre snit og en præcis manipulation og dissektion af vævene. I sidste ende reducerede disse teknologiske fremskridt kirurgiske traumer, sår- og hæmoragiske komplikationer og postoperative smerter, hvilket førte til en hurtigere bedring af patienten. Rosales et al. rapporterede oplevelsen af den første laparoskopinyretransplantation[2], som blev udførligt beskrevet af Modi et al. i en serie på 72 patienter [3]. Forfatterne konkluderede, at laparoskopisknyretransplantationer muligt og garanterer betydeligt færre postoperative smerter, men kræver en stejl indlæringskurve.

cistanche mandlige fordele
Startende fra begyndelsen af 2000'erne revolutionerede robotkirurgi minimalt invasiv kirurgi og løste de to vigtigste problemer med laparoskopi, nemlig bidimensionelt syn og manglen på artikulerende instrumenter. Brugen af instrumenter med syv frihedsgrader og med et tredimensionelt kamera med en tidoblet zoomstyrke er særligt afgørende ved præcise operationer som dem, der involverer vaskulære anastomoser. I 2002 beskrev Hoznek et al. robotassisterede vaskulære og ureterovesikale anastomoser [4·]. Giulianotti og Oberholzer beskrev håndassisteretrobot-assisteret nyretransplantation(RAKT) i en serie af overvægtige patienter [5, 6]. I 2014 rapporterede Menon et al. om teknikken til RAKT(Robot-assisteret nyretransplantation)i en kohorte på 25 på hinanden følgende patienter.
I 2015, en multi-institutionel gruppe inden for EAU Robotic Urology Section (ERUS-RAKT)(Robot-assisteret nyretransplantation)Arbejdsgruppe) blev nedsat i Europa. Som følge heraf blev en prospektiv serie på 120 patienter offentliggjort i 2017, som i øjeblikket har indskrevet mere end 300 patienter [7·e].
Kirurgisk teknik
Den kirurgiske teknik blev standardiseret af Menon et al. [8·e]. Forfatterne beskrev en transperitoneal tilgang, selvom den ekstraperitoneale har vist sig at være gennemførlig [9]. Litotomipositionen bruges med en 20-30 graders Trendelenburg-hældning. Indledningsvis indsættes tre 8-mm robottrokarer med en 12-mm assisterende trokar. Teknikken foreslået af ERUS-RAKT(Robot-assisteret nyretransplantation)Arbejdsgruppen angiver positionen af den tredje trokar ved krydset mellem spin-ombilical line og pubis-fjerde arm linje med DaVinci Si, mens brugen af DaVinci Xi tillader at sætte trokaren inline(Fig.1)[100]. De ydre iliaca-kar forberedes, og der skabes en peritoneal pose til transplantatet. Derefter dissekeres den forreste blærevæg indtil slimhinden til forberedelse af den ureterovesikale anastomose. For at sikre regional hypotermi af transplantatet kan nyren være omgivet af en gaze-jakke fyldt med isslam på bænken efter ureteral stentplacering og karforberedelse. Derefter udføres et periumbilical 6-cm snit, og transplantatet indføres via en GelPOINT@, hvor kameratrokaren og en anden 12-mm assisterende trokar placeres. Alternativt kan transplantatet indføres via et Pfannenstiel-snit[11. Hos kvindelige modtagere kan nyren også indføres via en intravaginal indsættelse [12]. Efter indføringen af transplantatet, i bughulen, kan isslam leveres til transplantatet gennem Gel-POINT@ hvert 15. minut for at opretholde hypotermi.
Den ydre iliaca-vene klemmes fast med to bulldogs, og efter venotomien anastomeres den med den podede vene på en kontinuerlig ende-til-side-måde ved hjælp af en 6/0 Gore-Tex国(fig.2A-C) ). Efter fastklemning af den ydre iliaca arterie udføres lineær arteriotomi og kan omdannes til en cirkulær arteriotomi via en aorta-punch eller med en saks. Teknikken til arteriel anastomose ligner venøs anastomose (fig. 2D-F). Ureteroneocystostomien udføres i henhold til Lich-Gregoir-teknikken med 5/0 monofilamentsutur (fig. 2G-I). Efter declamping og evaluering af korrekt transplantatperfusion retroperitonealiseres nyren. Bughinden lukkes med hemlocks, så dens permeabilitet mindsker risikoen for lymfocele i det postoperative forløb. Ydermere ligner transplantatets ekstraperitonealisering den åbne teknik og giver nem adgang til nyren for perkutan biopsi eller nefrostomirørplacering [13].
Intraoperative resultater
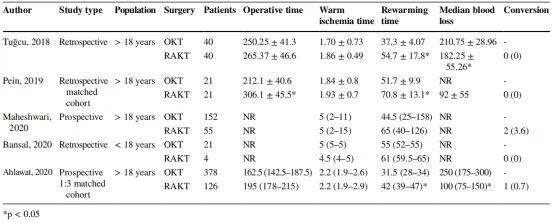
Menon et al. påvist, at RAKT(Robot-assisteret nyretransplantation)var muligt med en samlet operationstid (middel±standardafvigelse) på 214,1 ±39,8 min. og en genopvarmningstid på 46,6±9,3 min. Breda et al. bekræftede disse resultater og fandt genopvarmningstiden<48 min="" was="" correlated="" with="" better="" renal="" function="" recovery="" on="" postoperative="" day="" 30="" [7··].="" to="" date,="" few="" studies="" compared="" the="" outcomes="" of="">(Robot-assisteret nyretransplantation)versus OKT i retrospektive eller prospektive serier (tabel 1). Forfatterne fandt, at operationstid og genopvarmningstid var signifikant højere i RAKT(Robot-assisteret nyretransplantation)gruppe. På den anden side var medianblodtab lavere med robottilgangen med en 0.7-3,6 procent af konverteringsraten.
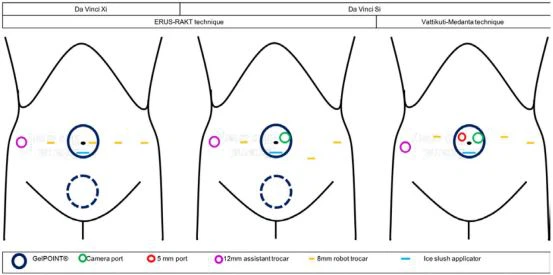
Fig. 1 ERUS-RAKT trokarpositionering for Da Vinci Si/Xi robot med periumbilical (Pfannenstiel; stiplet cirkel) snit og original Vattikuti Medanta teknik
Postoperative resultater
Breda et al. rapporterede en komplikationsrate på 19 procent (23/120) og 7,5 procent (9/120) Clavien-Dindo Større end eller lig med 3 komplikationer[7·]. Median postoperativ eGFR efter 30 dage var 52,6 ml/min. Positive resultater blev bekræftet ved 1-års opfølgning [19]. Resultaterne af den opdaterede serie, der tilmelder 291 levende donor RAKT(Robot-assisteret nyretransplantation),confirmed arate of 7.5%(22/291)Clavien-Dindo≥3 complications with 5/291(1.7%)delayed graft function (DGF),2/291(0.7%)embolization,3/291(1%)transplant-ectomies for arterial thrombosis, 3/291(1%)transplantec-tomies for vein thrombosis,6/291(2%)bleedings requiring surgical exploration,2/291(0.7%) ileus requiring surgical exploration,and 1/291(0.3%) transplantectomies for acute rejection.Late complications(>90 dage) omfattede 9/291 (3 procent) lymfocytter, 6/291 (2 procent) ureterisk stenose og 3/291 (1 procent) incisionsbrok.
Tabel 2 beskriver de postoperative resultater i sammenlignende serier med en opfølgning på 6-31 måneder.
Tre undersøgelser rapporterede signifikant højere brug af morfinderivater i OKT-gruppen [16,17,18·e], mens Tugcu et al. demonstrerede mindre postoperativ smerte i RAKT(Robot-assisteret nyretransplantation)gruppe i løbet af de første 24/48 timer[14]. En højere frekvens af sårinfektioner blev rapporteret i OKT-serien. I en prospektiv matchet kohorte på 504 patienter, Ahlawat et al. viste signifikant flere sårinfektioner (4 procent vs. 0 procent) og symptomatiske lymfocytter (7 procent vs. 0 procent) i OKT versus RAKT(Robot-assisteret nyretransplantation)DGF- og kreatininniveauer ved sidste opfølgning var sammenlignelige i alle serier. Længden af hospitalsophold blev rapporteret som lavere i RAKT(Robot-assisteret nyretransplantation)tilfælde [15] eller sammenlignelige blandt grupper[17,18·], ifølge forskellige kilder.
Tabel 1 Kirurgiske resultater i sammenlignende serier af robotassisteret nyretransplantation (RAKT) og åben nyretransplantation (OKT)
Komplekse kirurgiske scenarier Overvægtige patienter
Fedme er en velkendt risikofaktor for sårinfektioner, som er karakteristiske for immunkompromitterede patienter [20]. Infektioner på operationsstedet har vist sig at være en uafhængig risikofaktor for tab af transplantat. Lynch et al. rapporterede en dramatisk forskel i 3-års graftoverlevelse hos modtagere med eller uden en sårinfektion (70 procent mod 88 procent)[20]. Derudover kan den immunaktivering, der genereres af en infektion, spille en rolle ved graftafstødning [21]. Derfor er implementering af en minimalt invasiv teknik, der har potentiale til at mindske risikoen for sårinfektioner hos overvægtige patienter, relevant. Desuden RAKT(Robot-assisteret nyretransplantation) might increase the number of patients eligible for KT, as BMI>35 kg/m2 betragtes som en relativ kontraindikation i nogle lande.
I 2013 rapporterede Oberholzer et al. et relevant fald i infektioner på operationsstedet hos 28 overvægtige patienter (gennemsnitlig BMI43±7,8 kg/m2) indsendt til RAKT(Robot-assisteret nyretransplantation)og sammenlignet med en frekvensmatchet retrospektiv kohorte (29 procent vs. 0 procent ;p=0.004).Ved 6-måneders opfølgning kunne nyrefunktionen overlejres (p{{7} }.47), DGF(p=0.99),akut afstødning(p=0.99), og 100 procent af transplantatoverlevelsen blev fundet [6]. Den samme gruppe sammenlignede RAKT(Robot-assisteret nyretransplantation)modtagere (n=67) til OKT-modtagere fra United Network of Organ Sharing-databasen (n=545). Patientoverlevelsesraterne ved 1 år (96,8 og 98 procent) og 3 år (97 og 95 procent). ) var ikke forskellig mellem RAKT(Robot-assisteret nyretransplantation)henholdsvis OKT-modtagere. Transplantatoverlevelsesrater var også ens [22].
For nylig har Prudhomme et al. rapporterede data fra ERUS-RAKT(Robot-assisteret nyretransplantation)Arbejdsgruppe.I alt 169 levende donor RAKT(Robot-assisteret nyretransplantation)blev stratificeret efter BMI (BMI<25><><30 kg/m2;bmi="">30 kg/m2). Median eGFR ved 1-års opfølgning var 54(45-60),57(46-70) og 63(49-78)ml/min/1,73 m2 hos henholdsvis fede, overvægtige og ikke-overvægtige modtagere(p=0.5). Hyppigheden af postoperative komplikationer og DGF afveg ikke signifikant i de tre grupper [23]. Spørgsmålet om, hvorvidt samtidig RAKT(Robot-assisteret nyretransplantation)og ærmegatrektomi til vægttab ville blive en mulig mulighed i fremtiden forbliver ubesvaret, selvom den kombinerede procedure allerede er beskrevet [24].

cistanche mandlige fordele
Flere fartøjer
To undersøgelser behandlede resultaterne af RAKT(Robot-assisteret nyretransplantation) ved hjælp af graft med flere kar. Siena et al. analyserede ERUS-RAKT(Robot-assisteret nyretransplantation)database og sammenlignede 21 RAKT'er(Robot-assisteret nyretransplantation)med flere fartøjer til 127 RAKT'er(Robot-assisteret nyretransplantation)med enkelte fartøjer. Den vaskulære rekonstruktion blev udført på bænkbordet: teknikkerne blev forenet (pantaloon-måde), genimplantation (ende-til-side) af den polære arterie i hovednyrearterien eller en kombination af begge. De fandt, at de totale og kolde iskæmitider var signifikant længere i kohorten med flere kar (henholdsvis 112 vs. 88 min, p=0.004 og 50 vs. 34 min., p=0.003), mens ingen forskel blev fundet for genopvarmning og anastomose tid. Ved 30-dagsopfølgning, RAKT(Robot-assisteret nyretransplantation)brug af transplantation af flere kar var ikke en forudsigelse for suboptimal nyrefunktion (eGFR<45 ml/min/1.73="" m2)[25].="" on="" the="" other="" hand,="" prudhomme="" et="" al.="" found="" the="" number="" of="" graft="" arteries="" was="" independently="" associated="" with="" suboptimal="" renal="" function="" at="" postoperative="" day="" 30(or="0.71;" ci;p="0.02)in" obese="" recipients="" [23].="" nataraj="" et="" al.="" matched="" 43="">(Robot-assisteret nyretransplantation)med 43 OKT'er ved hjælp af multiple kar-transplantater. I denne undersøgelse blev vaskulær rekonstruktion udført enten ekstrakorporal eller intrakorporal. De fandt, at det gennemsnitlige analgetiske behov, postoperative smerter (2. POD) og hospitalsophold var signifikant lavere i RAKT(Robot-assisteret nyretransplantation)gruppe (alle s<0.05). postoperative="" complications="" were="" similar,="" except="" for="" wound-related="" events="" which="" were="" more="" frequent="" in="" the="" okt="" group="" (4.2%="" vs="" 0%;="" p="0.002)and" ileus="" which="" was="" more="" frequent="" in="" the="">(Robot-assisteret nyretransplantation)gruppe(18,6 procent mod 2,3 procent ;p =0.001). Funktionelle resultater var ens mellem RAKT(Robot-assisteret nyretransplantation) og OKT-grupper (henholdsvis eGFR62.4 vs. 61.8 ml/min/1.73 m2; p=0.9) ved 6-måneders opfølgning [26].
Indlæringskurve
To undersøgelser analyserede indlæringskurven i RAKT(Robot-assisteret nyretransplantation), begge ved at anvende den statistiske proceskontrolmetode [27]. Ahlawat et al. sammenlignede 33 RAKT'er(Robot-assisteret nyretransplantation)udført af en naiv kirurg til 64 RAKT'er(Robot-assisteret nyretransplantation) from the reference center. However, the index sur-geon had a significant previous experience in robotic surgery (n>500) og OKT(n=450). Analysen fokuserede på kirurgisk tid, vaskulære anastomoser og genopvarmningstid. Kompetencen kunne opnås inden for 10 tilfælde med forbedret færdighed og gennemsnitlig kirurgisk tid efter 20-25 tilfælde. Kortsigtede funktionelle resultater blev ikke ændret af øget erfaring[28]; ikke desto mindre er det vigtigt at huske den relativt lille stikprøvestørrelse af en sådan undersøgelse for at forhindre en formel indlæringskurveanalyse. ERUS-RAKT(Robot-assisteret nyretransplantation) group provided the analysis of learning curves from five centers with>20 RAKT'er(Robot-assisteret nyretransplantation).Det viste sig, at komplikationer og DGF faldt signifikant efter de første 20 tilfælde. Forfatterne bekræftede, at genopvarmningstid ikke var en forudsigelse for kortsigtede funktionelle resultater. Derfor blev en trifecta foreslået (ingen større intra/postoperative komplikationer, ingen DGF og genopvarmningstid
Vigtigheden af proctorship under overgangen fra OKT til RAKT(Robot-assisteret nyretransplantation)er nøglen. I denne opfattelse organiserede ERUS specifik hands-on træning i prækliniske modeller i analogi med andre etablerede træningsveje dedikeret til robotkirurgi [29,30]. Desuden foreslog Saba et al. for nylig en RAKT(Robot-assisteret nyretransplantation)simuleringsplatform, der bruger 3D-print og hydrogelstøbningsteknologier, der skal bruges inden for en tre-trins protokol: observatørskab ved højvolumencentret, da Vinci kirurgi online træning og endelig afslutning af fire simulerede procedurer, inklusive donornefrektomi og RAKT(Robot-assisteret nyretransplantation) [31].
Fremtidsperspektiver Udvidende indikationer for RAKT(Robot-assisteret nyretransplantation)
Indikationerne for RAKT(Robot-assisteret nyretransplantation)er steget de seneste år. De indledende rapporter udelukkede patienter med signifikant iliaca-arterosklerose, tidligere historie mednyretransplantation, tidligere større abdominalkirurgi, høj risiko for afstødning og dobbelt-/multiorgan-recipienter [8·e]. Oberholzer et al. omfattede patienter med tidligerenyretransplantationeller høj risiko for afvisning [6]. Det er også blevet påvist mulig at udføre samtidige bugspytkirtel/nyretransplantationer, dobbeltnyretransplantationer eller ortotopiskenyretransplantation[32-34]. De vigtigste udfordringer vedrører implementeringen af RAKT(Robot-assisteret nyretransplantation)i afdøde donorprogrammer og inklusion af patienter, der er ramt af svær iliaca-arterosklerose. I det første tilfælde viste en undersøgelse fra gruppen af Firenze dets gennemførlighed med transplantationscentre, der har erfaring med robotkirurgi, og det største problem vedrører tilgængeligheden af robotplatformen i en presserende situation [35]. I sidstnævnte tilfælde er tabet af robotter. haptisk feedback under RAKT(Robot-assisteret nyretransplantation)udelukker nøjagtig intraoperativ vurdering af ateromatiske plaques og øger risikoen for utilstrækkelig vaskulær kontrol ved brug af klemmer. Fremskridtene inden for teknologi og især inden for augmented reality-kirurgi kan overvinde det væsentlige problem og udvide indikationen af RAKT(Robot-assisteret nyretransplantation)til langtidsdialysemodtagere.
cistanche mandlige fordele
Intrakorporale graft kølesystemer
Opvarmningstiden er afgørende under RAKT(Robot-assisteret nyretransplantation), fordi temperaturen i bughulen hurtigt kan øge transplantattemperaturen. Derfor er de funktionelle resultater af RAKT(Robot-assisteret nyretransplantation)kan teoretisk set være mere afhængig af genopvarmningstiden end OKT [36]. Dette ville være endnu mere overbevisende i RAKT(Robot-assisteret nyretransplantation)fra afdøde donorer, for hvem den samlede iskæmi-tid uvægerligt er længere, og som følge heraf kan iskæmi-reperfusionsskaden være større. Af denne grund blev den regionale hypotermi-teknik introduceret af Menon et al. Det skal bemærkes, at transplantatets middeltemperatur var 20,3±2,9 minutter, således at den intrakorporale afkøling gjorde det muligt at opretholde en acceptabel, men ikke optimal, nyretemperatur [8··]. Desuden øger påføringen af knust is på transplantatet risikoen for ileus [26]. Ganpule et al. foreslået en modificeret jakke, hvor isen blev placeret i to rum af en fire-lags gaze for at undgå direkte kontakt med tyndtarmen[37]. På nuværende tidspunkt er den nuværende dokumentation for de intrakorporale kølesystemer sparsom. To undersøgelser rapporterede dedikerede kølesystemer i en svinemodel. En termisk barrierepose blev fundet at reducere hastigheden af temperaturændringer under RAKT(Robot-assisteret nyretransplantation), selvom det efter 40 minutter var lidt mindre end 30 grader C [38].
Meier et al. rapporterede resultaterne af en nyrejakke af silikone, der kontinuerligt var gennemstrømmet af methylenblåt og ethanol ved 4 grader. Reperfusionstemperaturen under RAKT(Robot-assisteret nyretransplantation)med silikonejakken var 6,5 graders grader sammenlignet med 28,7 grader C under RAKT(Robot-assisteret nyretransplantation)uden køling eller 22,5 grader under OKT. Histologi og MR viste mindre alvorlige iskæmi-reperfusionslæsioner og parenkymal heterogenitet i de afkølede graftgrupper. Systemet blev aldrig testet i en menneskelig model og havde to store ulemper. Brugen af ethanol til køling er tvivlsom, da der er risiko for antændelse ved brug af energiapparater. Posen øger transplantatets samlede dimension markant, hvilket kan påvirke snitlængden og ergonomien under operationen [39].
For nylig har en kold iskæmi-anordning vist sig at opretholde en lav grafttemperatur under operationen gennem de IDEALE faser 0 og 1. Specielt viste enheden gennemførlighed for både OKT og RAKT(Robot-assisteret nyretransplantation)hos mennesker, og transplantattemperaturen oversteg aldrig 20 grader (middeltemperatur: OKT 15,7C vs RAKT(Robot-assisteret nyretransplantation)18,3 grader )[40].
Omkostninger
Omkostningerne ved implementeringen af en RAKT(Robot-assisteret nyretransplantation)programmet er væsentligt, om robotplatformen endnu ikke er tilgængelig i centret. Så de institutioner, der allerede har eksperimenteret med proceduren, er alle højvolumencentre med en bred erfaring inden for robotkirurgi. Derudover bestemmer robottens engangsforbrugsstoffer andre ekstra omkostninger pr. procedure. Til dato er der ikke foretaget nogen cost-benefit-analyse for at sammenligne RAKT og OKT. Oberholzer et al. rapporterede en forskel pr. procedure på 15000 USD, uden at tage højde for omkostningerne ved købet af robotten [6]. Hameed et al. omkostninger til operationsstuen svarede til robotassisterede radikale prostatektomier (10000 USD)[41].
På den anden side det postoperative forløb efter RAKT(Robot-assisteret nyretransplantation)kan drage fordel af en minimalt invasiv teknik og dermed reducere omkostningerne og potentielt føre til omkostningsneutralitet efter et specifikt antal procedurer[42]. Det forventes, at markedsføringen af nye robotplatforme reducerer omkostningerne til robotten og dens engangsartikler.
Konklusioner
Aktuelle beviser viser, at RAKT(Robot-assisteret nyretransplantation)er sikker og gennemførlig i den levende donation og giver lignende funktionelle resultater ved midtvejsopfølgning, både hos overvægtige og normalvægtige patienter. Et randomiseret kontrolleret forsøg er nødvendigt for endeligt at bekræfte resultaterne af retrospektive og prospektive kohortestudier. Implementeringen af proceduren i flere centre afhænger af udvidelsen af kirurgiske indikationer, hvilket også kan reducere omkostningerne. For at garantere anvendeligheden af RAKT(Robot-assisteret nyretransplantation)fra afdøde donorer er det fundamentalt at anvende graftkølesystemer og at inkludere modtagere med ateromatøse iliaca arterier.
Referencer
Artikler af særlig interesse, der er offentliggjort for nylig, er blevet fremhævet som: ●Af betydning ●●Af stor betydning
1. Faba OR, Boissier R, Budde K, Figueiredo A, Taylor CF, Hevia V, et al. European Association of urology guidelines on renal trans-plantation: update 2018.Eur Urol Focus.2018;4:208-15.https://doi.org/10.1016/j.euf.2018.07.014.
2.●Rosales A, Salvador JT, Urdaneta G, Patino D, Montlle6 M, Esquina S, et al. Laparoskopisknyretransplantation. Eur Urol.2010;57:164-7.https://doi.org/10.1016/j.eururo.2009.06. 035. Den første beskrivelse af laparoskopisknyretransplantation.
3.Modi P,Pal B,ModiJ,Singla S,Patel C,Patel R, et al.Retroperi-toneoskopisk levende-donor nefrektomi og laparoskopisknyretransplantation: erfaring med indledende 72 sager. Transplantation. 2013;95:100-5.https://doi.org/10.1097/TP.0b013e3182795bee.
4. ● Hoznek A, Zaki SK, Samadi DB, Salomon L, Lobontiu A, Lang P, et al.Robot-assisteret nyretransplantation: an initial experience.J Urol.2002;167:1604-6.Den første beskrivelse af roboticnyretransplantation.
5. Giulianotti P, Gorodner V, Sbrana F, TzvetanovI, Jeon H, Bianco F, et al. Robotisk transabdominalnyretransplantationhos en sygeligt overvægtig patient. AmJ Transplant.2010;10:1478-82.https://doi.org/10.1111/j.1600-6143.2010.03116.x.
6. OberholzerJ, Giulianotti P, Danielson KK, Spaggiari M, Bejarano-Pineda L, Bianco F, et al. Minimalt invasiv robotnyretransplantationfor overvægtige patienter tidligere nægtet adgang til transplantation. Am JTransplant.2013;13:721-8.https://doi.org/10.1111/ajt.12078.
7.··Breda A, Territo A, Gausa L, Tugcu V, Alcaraz A, Mosquera M, et al.Robot- assisteretnyretransplantation: den europæiske erfaring. Eur Urol.2018;73:273-81.https://doi.org/10.1016/i. eururo.2017.08.028. Det første multicenter ikke-randomiserede forsøg medrobot-assisteret nyretransplantation.
8.··Menon M, Sood A, Bhandari M, Kher V, Ghosh P, Abaza R, et al. Robotisknyretransplantationmed regional hypotermi: en trin-for-trin beskrivelse af Vattikuti Urology Institute-Medanta-teknikken (IDEAL fase 2a). Eur Urol.2014;65:991 1000.https://doi.org/10.1016/j.eururo.2013. 12.006.Robot-assisteret nyretransplantationteknik ved hjælp af regional hypotermi.
9.Tsai MK, Lee CY, Yang CY, Yeh CC, Hu RH, Lai HS. Robot-assisteret nyretransplantation i retroperitoneum. Transpl Int. 2014;27:452-7.https://doi.org/10.1111/tri.12279.
10. Gallioli A, Territo A, Boissier R, CampiR, Vignolini G, Mosquera M, et al. Læringskurve indrobot-assisteret nyretransplantation: resultater fra arbejdsgruppen European Robotic urological Society.Eur Urol.2020.https://doi.org/10.1016/j.eururo.2019.12. 008.Læringskurven afrobot-assisteret nyretransplantationifølge de europæiske erfaringer.
11. Vignolini G, Greco I, Sessa F, Gemma L, Pecoraro A, Barzaghi P, et al. Universitetet i Firenze teknik tilrobot-assisteret nyretransplantation: 3-Års erfaring. Front Surg. 2020;7:583798.https://doi.org/10.3389/fsurg.2020.583798.
12. Doumerc N, Roumiguié M, Rischmann P, Sallusto F. Fuldstændig robottilgang med transvaginal indsættelse fornyretransplantation. Eur Urol. 2015;68:1103–4. https://doi.org/10. 1016/j.eururo.2015.07.026.
Bemærk:ovenstående er ikke en fuldstændig referenceliste
