Forskellige typer af kronisk nyresygdom (CKD), du behøver at vide
Mar 22, 2022
ali.ma@wecistanche.com
Del Ⅱ: Urinprotein- og peptidmarkører ved kronisk nyresygdom
Natalia Chebotareva, Anatoliy Vinogradov & et al.
Abstrakt
Kronisk nyresygdom (CKD)er en uspecifik typenyre sygdomsom forårsager et gradvist fald i nyrefunktionen (fra måneder til år). CKD(Kronisk nyresygdom)er en væsentlig risikofaktor for død, hjerte-kar-sygdomme og nyresygdom i slutstadiet. CKD'er(Kronisk nyresygdom) af forskellig oprindelse kan have de samme kliniske og laboratoriemanifestationer, men forskellige progressionshastigheder, hvilket kræver tidlig diagnose at bestemme. Denne gennemgang fokuserer på protein/peptid biomarkører for de førende årsager til CKD(Kronisk nyresygdom): diabetisk nefropati, IgA nefropati, lupus nefritis, fokal segmental glomerulosklerose og membranøs nefropati. Massespektrometri (MS)-tilgange gav mest information om urin-peptid- og proteinindhold i forskellige nefropatier. Nye analytiske tilgange gør det muligt at bruge urinproteomiske peptidprofiler som tidlige ikke-invasive diagnostiske værktøjer til specifikke morfologiske former fornyre sygdomog kan blive et sikkert alternativ til nyrebiopsi. MS-studier af de vigtigste patogenetiske mekanismer for udvikling af nyresygdom kan også bidrage til at udvikle nye tilgange til målrettet terapi.

Klik for at cistanche tubulosa fordele og bivirkninger og for nyresygdom
KLIK HER FOR AT DELTAⅠ & Ⅲ
4. Membranøs nefropati
Membranøs nefropati(MN) er en førende årsag til nefrotisk syndrom (NS) hos voksne. Denne sygdom har en autoimmun natur, hvilket blev bekræftet af tilstedeværelsen af autoantistoffer mod podocytantigener, herunder antistoffer mod phospholipase A2-receptorer (aPLA2R) og trombospondin 1-domæneholdig 7A (THSD7A) [97,98]. De sekundære årsager til MN(Membranøs nefropati) omfatter stofbrug, infektioner, autoimmune sygdomme og cancer [99]. Den primære mekanisme af MN(Membranøs nefropati)er podocyt autoimmun beskadigelse af phospholipase A2 receptor antistoffer, hvilket fører til massiv proteinuri. Diagnosen og behandlingen af denne sygdom er i øjeblikket baseret på bestemmelsen af aPLA2R-antistoftiteren. Søgningen efter yderligere markører virker lovende i den aPLA2R-negative type af idiopatisk MN(Membranøs nefropati). MN(Membranøs nefropati)patientundersøgelser giver sammenlignende tværsnitsanalyser af proteomet i MN(Membranøs nefropati)sammenlignet med andre nefrotiske typer af nefritis og raske kontroller. Panelet af specifikke urinproteinmarkører, der skelner MN(Membranøs nefropati)fra andre nefropatier inkluderer nedsatte niveauer af zinkfingerprotein ZFPM2, E1A-bindende protein og mikrotubuli-associeret protein tauAP-3 kompleks subunit delta-1 [54], såvel som øgede niveauer af thyroxinbindende globulin (SERPINA7)[50], lysosommembranprotein-2(LIMP-2)[56], plasminogen [54], LDB3, PDLI5 [100] og afamin [55,57]. En sammenligning af prøver fra patienter med APLA2R-positiv MN og APLA2R-negativ MN, såvel som raske individer, afslørede signifikant højere niveauer af A1AT og hungersnød i den positive MN-gruppe [101]. En kombination af urinretinolbindende protein4 og SH3-domænebindende glutaminsyrerigt-lignende protein 3 kan differentiere MCD fra DN. På samme måde kan en kombination af urin afamin og komplement C3 urin/plasma-forhold skelne MN fra DN[55].

Generelt findes markører i MN(Membranøs nefropati)spiller en rolle i den klassiske vej med komplementaktivering og immunrespons, celleadhæsion, receptormedieret endocytose, blodpladedegranulering og koagulationskaskaden [57]. LIMP-2 spiller en central rolle i inflammatorisk immunresponsregulering i nyrevævet [56] og afspejler vævsinfiltration af immunceller. LMP-2 kan også hjælpe med at bestemme sygdomsaktivitet. LDB3- og PDL5-proteinerne spiller en rolle i modifikationen af podocytcytoskelettet, hvilket kan føre til proteinuri. Afamin, hvis forhøjelse er forbundet med idiopatisk MN(Membranøs nefropati), er den mest lovende specifikke MN(Membranøs nefropati)markør, da dens betydning blev bekræftet i flere undersøgelser (tabel 2).
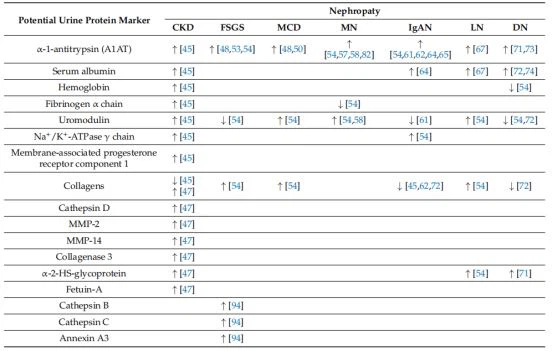
Tabel 2. Potentielle urinproteommarkører i forskellige nefropatier.
5. IgA nefropati
IgA nefropati(IgAN) er den mest almindelige form for kronisk glomerulær sygdom hos voksne. I Europa er frekvensen af IgAN(IgA nefropati) varierer fra 19 til 51 procent af de nyrebiopsier, der udføres for glomerulære sygdomme [102-104]. Patienter med lgAN har ofte øgede niveauer af IgA1 med galactose-deficiente O-glycaner i hængselregionen. Blodniveauerne af et afvigende glykosyleret IgA1 er højere i IgAN(IgA nefropati)end hos raske kontroller eller patienter med andrenyresygdomme. Produktionen af galactose-deficiente IgA1-antistoffer, dannelse af immunkomplekser og akkumulering af disse komplekser i mesangium blev vist at initiere nyreskade [105]. Desuden forstærkede aktiveringen af alternative komplementveje vævsskade [106]. Transferrinreceptor (CD71) på humane mesangiale celler kan binde immunkomplekser indeholdende galactose-deficient IgA [107].
Omkring 40 urinproteinmarkører, der differentierer IgAN(IgA nefropati) have been described, >20 af dem er kun specifikke for lgAN(tabel2). Niveauerne af komplement C9, Ig kappa kæde C-region og tre cytoskelet keratiner (type I(10) og type I(1 og 5)) ændrede sig synkront i glomeruli (biopsiprøve) hos lgAN-patienter sammenlignet med det intakte nyrevæv områder af patienter med tumorer [59]. Ændrede niveauer af 30 urinproteiner og fire potentielle markører (intercellulært adhæsionsmolekyle 1 (ICAMl), metalloproteinasehæmmer 1, antithrombin IIl og adiponectin) blev afsløret i IgAN(IgA nefropati) med lav proteinuri(<1 g/l)="" and="" stable="" renal="" function="" (glomerular="" filtration="" rate:57.3="" (23-106)ml/min).="" a="" larger="" multicenter="" study="" suggested="" that="" a="" decreased="" number="" of="" collagen="" fragments="" in="" the="" urine="" (specifically="" type="" i="" collagen)="" might="" be="" most="" informative="" in="" progressive="">IgA nefropati), på grund af nedsat kollagennedbrydning og kollagenasehæmning i nyrefibrose [62].

Andre potentielle lgAN-specifikke markører omfatter øgede niveauer af adiponectin 60], 2-makroglobulin, komplement C4a, prothrombin [63], antithrombin II [60,63], -1B-glycoprotein [64], glycoprotein 2, epidermal vækstfaktor, CMRF35-lignende molekyle, protocadherin, uteroglobin, dipeptidylpeptidase IV, NHL-gentagelsesholdigt protein 3 og CD84 [36] og nedsatte niveauer af fibulin-5, YIP1 familiemedlem 3 , der foreslår [108], aminopeptidase N [65] og LG3-fragmentet af endorse Pellin [64]. Det sidste var det eneste nedsatte protein i tungere IgAN(IgA nefropati)med en langsommere glomerulær filtrationshastighed [64]. Samtidig kan høje LG3-niveauer hæmme angiogenese og være ansvarlige for nyrefunktionstab i nogle andre IgAN(IgA nefropati)patienter [64]. Selvom data om ændringer i niveauet af vasorin er inkonsistente [36,65], kan det også betragtes som et specifikt IgAN(IgA nefropati)markør. Antithrombin I er især bemærkelsesværdig som den eneste specifikke IsAN-markør bekræftet i to uafhængige undersøgelser [60,63].

6. Diabetisk nefropati
Diabetisk nefropati(DN) påvirker omkring 30-40 procent af diabetes mellitus (DM) patienter og er den førende årsag til CKD(Kronisk nyresygdom)og nyresygdom i slutstadiet (ESRD) over hele verden, især i høj- og mellemindkomstlande. DN(Diabetisk nefropati)fører til glomerulær mesangial ekspansion; fortykkelsen af basalmembranen; og, karakteristisk, progressionen af nodulær glomerulosklerose på grund af glomerulær hyperfiltration [109.
Rækken af potentielle specifikke DN(Diabetisk nefropati) markers in the urine includes >10 proteiner (tabel 2), med øgede niveauer af vitamin D-bindende protein, calgranulin B, hæmoexin [71l, zink- 2-glycoprotein [71,74], 408 N-bundne glykoproteiner [73], cystatin C, ubiquitin, -1-syre glycoprotein 1, pigmentepitel-afledt faktor [74], Clara-celleprotein CC16 [76] og fi-bronectin [110], samt nedsatte niveauer af transthyretin [71,74] og forskelligt ændrede niveauer af -1 mikroglobulin/bicunin-precursoren (AMBP) [71,74,75].
Betydelige stigninger i urinniveauerne af B-glycoprotein(7-fold),zinkholdigt 2-glycoprotein(5.9-fold), 2-HSglycoprotein (4.{{ 8}} gange), vitamin D-bindende protein (4.8-fold), calgranulin B(3.9-fold), A1AT(2.9-fold) og hæmopexin ( 2.4-fold) pålideligt skelnen DN(Diabetisk nefropati)med makroalbuminuri fra DM uden albuminuri[71]. Omvendt et signifikant fald i transthyretin (4.3-fold), apolipoprotein A1 (3.2-fold), AMBP (1.6-fold) og retinolbindende plasmaprotein( 1.52-fold) blev observeret i DN(Diabetisk nefropati)med makroalbuminuri [71]. En modelundersøgelse med udvalgte proteiner antydede betydningen af cathepsin A, mucin 1, GM2 gangliosidaktivatoren, SPARC-lignende protein 1 og lysosomal sur phosphatase i den dårlige prognose for den tidlige udvikling af DN(Diabetisk nefropati)såvel som ved nyrefibrose [111]. En kombination af 408 N-bundne glycoproteiner, A1AT og ceruloplasmin viste sig at være i stand til at skelne mellem mikroalbuminuri og normoalbuminuri i DN(Diabetisk nefropati)patienter [73]. Urinary haptoglobin og AMBP kan skelne mellem diabetespatienter med og uden DN(Diabetisk nefropati)[75]. Den øgede udskillelse af 15,8 kDa Clara-celleprotein CC16 viste sig at være forbundet med proksimal tubuli dysfunktion hos DM-patienter med mikro- eller makroalbuminuri sammenlignet med DM-patienter uden albuminuri og raske kontroller [76]. Niveauerne af osteopontin og fibronectin var også højere i DN(Diabetisk nefropati)sammenlignet med dem i DM, og stigninger i urin neprilysin og VCAM-1 blev observeret efter losartanbehandling i DN(Diabetisk nefropati) [110].
En longitudinel undersøgelse af type 2 DM afslørede en stigning i urintransthyretin/pre-albumin og lg kappa C-kæderegionen inden for 0-5 år efter starten af DM; forekomsten af cystatin C og ubiquitin efter 5-10 år; og påvisning af -1-syre glycoprotein 1, apolipoprotein A1, AMBP, pigmentepitel-afledt faktor og zink -2-glycoprotein efter 10-20 år [74]. Den ikke-enzymatiske glykering af disse proteiner og deres peptider interfererer med normal tubulær reabsorption og kan føre til beskadigelse af de proksimale tubuli og direkte udskillelse af proteinerne i urinen.
Samlet set førnævnte DN(Diabetisk nefropati)markører kan afspejle processerne af tubulær atrofi og tubulointerstitiel fibrose, hvoraf mange er vigtige for DN(Diabetisk nefropati)prognose. Zink- 2-glycoprotein, transthyretin og AMBP bør særligt bemærkes, da deres prognostiske betydning blev bekræftet i mindst to uafhængige undersøgelser [71,74,75].
7. Lupus nefritis
Lupus nefritis(LN) er en af de mest almindelige og alvorlige komplikationer af systemisk lupus erythematosus og optræder normalt mindst 3-5 år efter sygdommens opståen. Mekanismerne for renal glomerulus-skade kan findes i aflejring af immunkomplekser eller autoantistoffer med efterfølgende komplementaktivering [112].LN(Lupus nefritis) fører til alvorlig nyreskade, der udvikler sig til nyresygdom i slutstadiet, hvis den ikke behandles tilstrækkeligt. Det vigtigste mål for LN(Lupus nefritis)behandlingen er dynamisk at vurdere graden af nyreskadeaktivitet, da de tilgængelige aktivitetsmarkører (daglig proteinuri, erytrocyturi, komplement og antinukleære antistoffer) ikke er informative. LN(Lupus nefritis)patienter skal i øjeblikket gennemgå flere nyrebiopsier for at overvåge LN(Lupus nefritis)aktivitet under immunsuppressiv terapi for at bestemme, hvor LN(Lupus nefritis)behandlingen skal fortsættes eller aflyses. I dette tilfælde er der behov for meget følsomme og specifikke LN(Lupus nefritis)markører i stand til at forudsige sygdomsforværring eller indikere utilstrækkelig effektivitet af behandlingen.
Kun få potentielle urinproteinmarkører, der er specifikke for LN(Lupus nefritis)kan noteres (tabel 2). Et par peptider, "3340" og "3980"(m/z), har gjort det muligt at differentiere et akut LN(Lupus nefritis)stand fra LN(Lupus nefritis)remission med 92 procent sensitivitet og 92 procent specificitet forud for ændringer i kliniske parametre (urinprotein/kreatinin-forholdet, antistoffer mod DNA, hæmaturi, serumkreatinin osv.). Desuden var disse peptider i stand til at forudsige tidligt tilbagefald og remission [66].
Særlige fragmenter af hepcidin, sammen med fragmenter af A1AT og albumin, blev fundet at være mere signifikante end systemisk lupus erythematosus renal flare cyklus LN(Lupus nefritis)i en dynamisk undersøgelse af urinproteomet [67l. Den ændrede ekspression af hepcidin 20 kan være en markør for nyreopblussen, hvorimod en stigning i hepcidin 25 efter behandling kunne bruges til at estimere effektiviteten af behandlingen [67].
Klassificeringen baseret på 172 peptider differentierede pålideligt92 LN(Lupus nefritis)tilfælde fra den generelle CKD(Kronisk nyresygdom)gruppe (1180 patienter) og identificerede proteinet S100-A9 som et andet specifikt LN(Lupus nefritis)markør, hvis øgede niveau viste sig at være afgørende for LN(Lupus nefritis)differentiering i kombination med øgede niveauer af kollagenpeptider og uromodulin, samt nedsatte niveauer af clusterin, -2-mikroglobulin og -2-HS-glycoprotein [54].
-1-Antichymotrypsin (SERPINA3) er et andet potentielt specifikt LN(Lupus nefritis)markør i urin og den eneste LN(Lupus nefritis)markør, hvis betydning blev bekræftet i to uafhængige undersøgelser [68,69]. Sammen med haptoglobin og retinolbindende protein blev SEPINA3 signifikant øget i aktivt LN(Lupus nefritis)sammenlignet med inaktivt LN(Lupus nefritis)[68]. Desuden viste SERPINA3 en moderat positiv korrelation med LN(Lupus nefritis)histologisk aktivitet, som blev bekræftet via immunhistokemi [69].
Generelt er det beskrevne LN(Lupus nefritis)markører gør det muligt at vurdere sygdommens aktivitet og ophobning af fibrose i nyrerne, hvilket er meget vigtigt i klinisk praksis ved behandling af patienter. De øgede niveauer af nogle proteiner kan tyde på tubulær dysfunktion under den akutte form af sygdommen [68].
8. Ikke-specifikke urinproteinmarkører
Uromodulin, kollagener, AlAT og deres fragmenter er de vigtigste ikke-specifikke urinproteinmarkører, der blev identificeret i alle de førnævnte nefropatier (tabel 2), såvel som i mange andre lidelser forbundet med nyreinsufficiens eller proteinuri [17-39] . Uromodulin er et nyrespecifikt glycosylphosphatidylinositol (GPI)-forankret glycoprotein, der udelukkende produceres af epitelcellerne, der beklæder den tykke opadgående lem af Henles løkke og er en normal komponent i urinen. Kollagenpeptider er også normalt til stede i urin og afspejler omsætningen af den ekstracellulære matrix i nyrevæv. Ikke desto mindre kan begge sædvanlige urinkomponenter indikere patologiske ændringer. Uromodulin kan også være en potentiel biomarkør, der er relevant for tubulær funktion og CKD(Kronisk nyresygdom)[113]. Niveauet af kollagenfragmenter korrelerer stærkt med initieringen af DN(Diabetisk nefropati)[13,17,19,45,72]; kvantitative ændringer i disse fragmenter i urinen blev observeret 3-5 år før udviklingen af makroalbuminuri [19]. Samlet set kan den kvalitative sammensætning af kollagenfragmenterne variere i forskellige nefropatier [45,47,54,72].
I modsætning til uromodulin- og kollagenpeptider er forekomsten af AlAT i urinen altid forbundet med en form for patologi og kan afspejle podocyt-stress [53]. Navnlig blev der observeret en stigning i urinalAT i alle nefropatierne, der blev gennemgået i denne undersøgelse (tabel 2).
Generelt forbedrede vurderingen af uspecifikke markører i kombination med specifikke markører signifikant differentieringen af nefropatier. Især niveauerne af seks UMOD- og A1AT-peptider differentierede mellem proliferative og ikke-proliferative (inklusive MCD, MN, FSGS og IgAN(IgA nefropati)) former for glomerulærnyresygdomme[58]. Desuden blev uromodulin-overekspression vist at disponere en for CKD'er(Kronisk nyresygdom)såsom hypertensiv nefropati og DN(Diabetisk nefropati)[114]. Påvisningen af kollagenfragmenter sammen med LG3-fragmentet af endorepellin er afgørende for diagnosticering af IgAN(IgA nefropati), da kollagen kan indikere et mere alvorligt sygdomsforløb med nedsat angiogenese og den hurtige udvikling af nyrefibrose [64]. Estimering af niveauerne af A1AT, uromodulin, transferrin, serumalbumin og -1- -glycoprotein er også vigtigt i lgAN, da sådanne niveauer afspejler almindelige patologiske processer, herunder øget apoptose, inflammation, koagulation og komplementaktivering [45,54, 61,62,64,65,72].
9. Konklusioner
Forskningsresultaterne indikerer det store potentiale i proteomisk analyse til non-invasiv diagnose afnyresygdomme, afklaring af de førende patogenetiske mekanismer for sygdomsprogression, og bestemmelse af handlingsmål til inhibering af sygdomsprogression. I modsætning til nyrebiopsi er urinproteomisk analyse sikker og pålidelig og kan gentages flere gange til overvågning af sygdom. Den proteomiske urinprofil giver værdifuld information om de førende patologiske processer, der forekommer i nyrevæv på undersøgelsestidspunktet.
Hovedtræk ved den proteomiske analyse er, at mange af de markører, der detekteres i urin, observeres som et resultat af proteingennemtrængning fra blodet (albumin, retinolbindende protein osv.) eller som refleksioner af almindelige patologiske processer såsom ekstracellulær matrixakkumulering (kollagener og A1AT), aflejring af immunoglobulinkomplekser, komplementaktivering, apoptose, lipidoxidation og tubulær dysfunktion (-2-mikroglobulin, uromodulin osv.) med høj proteinuri. I dette tilfælde er det afgørende at vurdere kvantitative ændringer i disse indikatorer for nøjagtigt at afspejle behandlingsaktiviteten og skadens alvor.
Et af de vigtigste mål for urinproteomisk analyse hos patienter med CKD(Kronisk nyresygdom)er at bestemme sygdomsspecifikke biomarkører eller deres kombinationer. Proteiner ekstraheret for første gang kræver størst opmærksomhed, da de kan afspejle de vigtigste patogenetiske stadier i sygdomsudvikling. For eksempel kan CD44, en markør for aktiverede parietale epitelceller, afspejle processerne af glomerulosklerose i MN[50] eller IgAN(IgA nefropati)[38]men kan på samme tid også være en væsentlig egenskab til at differentiere FSGS fra MCD [52]. DPEP1, primært identificeret i FSGS, menes at afspejle TRPC6-aktivering i podocytter [52];ubiquitin-60S ribosomalt protein L40 (UBA52), som er en markør for cellulær stress; eller komponenter af podocytcytoskelettet, der er beskadiget af antistoffer [49,115]. Apolipoproteiner, som kan spille en potentiel rolle i FSGS-patogenese som "permeabilitetsfaktorer"]116l, såvel som proteiner, hvis roller endnu ikke er fuldstændigt forstået, såsom lysosommembranprotein-2 og afamin i MN[56,57] og det laminin G-lignende 3(LG3)-fragment af endorse Pellin i IgAN(IgA nefropati)[64], kan afspejle patologiske processer og kan blive mål for nye tilgange til immunsuppressiv eller nefroprotektiv terapi. Derudover kan positive dynamiske ændringer i den proteomiske profil efter den udpegede terapi være med til at bekræfte, om de ordinerede medicin blev valgt korrekt og hjælper med at opnå de ønskede resultater. Men på trods af valideringen af CKD(Kronisk nyresygdom)273 klassificerer i flere undersøgelser, er der behov for at videreudvikle nye paneler med øget specificitet for specifikke nefropatier. Dette synes at være det vigtigste mål for yderligere proteomikforskning.
Referencer
1. Nyre sygdomForbedring af globale resultater (KDIGO).KDIGO kliniske retningslinjer for glomerulonefritis;NyreInternationale kosttilskud; Nature Publishing Group: New York, NY, USA, 2012.
2. National Kidney Foundation.K/DOQI klinisk praksis retningslinjer forkronisk nyresygdom: Evaluering, klassificering og stratificering. Er. J. Kidney Dis.2002, 39, 1-266.
3.Sarnak, MJ;Levey, AS;Schoolwerth, AC;Coresh, J;Culleton,B.; Hamm, LL; McCullough, PA; Kasiske, BL; Kelepouris, E.; Kag, MJ; et al.Nyre sygdomsom en risikofaktor for udvikling af hjerte-kar-sygdomme. Oplag 2003, 108, 2154-2169. [CrossRef] [PubMed]
4. Alani, H: Tamimi, A.; Tamimi, N. Kardiovaskulær co-morbiditet ikronisk nyresygdom: Aktuel viden og fremtidige forskningsbehov. World J. Nephrol.2014, 3, 156-168. [CrossRef] [PubMed]
5. Hsu, C; Ordonez, J: Chertow, G.; Fan, D.; McCulloch, C.; Go, A. Risikoen for akut nyresvigt hos patienter medkronisk nyresygdom. Nyre Int.2008, 74, 101-107. [CrossRef] [PubMed]
6. Tonelli, M.; Wiebe, N.; Culleton, B.; Hus, A.; Rabbat, C.; Fok, M.; McAlister, F; Garg, AXKronisk nyresygdomog Mortalitetsrisiko: En systematisk gennemgang. J. Am. Soc. Nephrol.2006, 17, 2034-2047. [CrossRef]
7. Hsu. C.-Y: Iribarren, C; McCulloch, CE; Darbinian, J.; Go, ASRisk Factors for End-StageRenalSygdom: 25-års opfølgning. Arch. Praktikant. Med. 2009,169, 342-350. [CrossRef]
8. Hill, NR; Fatoba, ST; Ok, JL; Hirst, J.; O'Callaghan, CA; Lasserson, D.; Hobbs, R. Global udbredelse afKronisk nyresygdom— En systematisk gennemgang og meta-analyse. PLoS ONE 2016, 11, e0158765. [CrossRef]
9, Schieppati, A.; Remuzzi, G. Kroniske nyresygdomme som et folkesundhedsproblem: Epidemiologi, sociale og økonomiske implikationer. Nyre Int.2005, 68, S7-S10. [CrossRef]
10. Bommer, J. Udbredelse og socioøkonomiske aspekter afkronisk nyresygdom. Nephrol.Dial. Transplant.2002, 17,8-12.[CrossRef]
11. Vos, T.; Allen, C.; Arora, M; Barber, RM; Bhutta, ZA; Brown, A.; Carter, A.; Casey, DC; Charlson, FJ.; Chen, AZ; et al. Global, regional og national forekomst, prævalens og leveår med handicap for 310 sygdomme og skader, 1990-2015: En systematisk analyse for Global Burden of Disease Study 2015.Lancet 2015, 388, 1545-1602. [CrossRef]
12. Dhaun, N.; Bellamy, CO; Cattran, DC; Kluth, DCUtilitet af nyrebiopsi i den kliniske behandling afnyresygdom. NyreInt. 2014, 85, 1039-1048. [CrossRef] [PubMed]
