Hvad er forholdet mellem nyreepitelmålrettet mitokondriel transkriptionsfaktor A-mangel med polycystisk nyresygdom--Del II
Mar 13, 2022
Kontakt:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Klik her for information om del I (Introduktion, materialer og metoder) i denne artikel.
Nyreepitel-målrettet mitokondriel transkriptionsfaktor A-mangel resulterer i progressiv mitokondriel udtømning forbundet med den alvorlige cystiske sygdom--Del II
Ken Ishii1,2,11et al.
DISKUSSION
Her etablerer vi en kritisk funktion for mt-transkriptionsfaktor TFAM i nyrevævshomeostase. Vi demonstrerer, at inaktiveringen af TFAM i SIX2, men ikke i HOXB7 progenitorceller, resulterede i udviklingen af alvorlig postnatal cystisk sygdom, som var forbundet med mt-depletering og et metabolisk skift fra OXPHOS mod glykolyse. Desuden er et fald i cellulære TFAM-niveauer og mt-dysfunktion karakteristiske træk ved murin og human PKD(polycystisk nyresygdom), hvilket tyder på, at en reduktion i TFAM-aktivitet kan bidrage til og/eller modulere udviklingen af nyrecystisk sygdom.
Patienter med mt sygdomssyndromer er tilbøjelige til at udvikle signyrepatologi.Nyre sygdomi denne indstilling viser sig ofte som tubulær dysfunktion og/eller tubulointerstitiel sygdom, hvorimod nyrecystedannelse er sjælden.12,19 22 Selvom mutationer i TFAM-regulerede gener, såsom MT-CO1, 23 er blevet identificeret hos patienter med tubulointerstitiel sygdom, er mutationer i selve TFAM ikke blevet rapporteret hos patienter med kroniskenyre sygdom. Ikke desto mindre er kronisk nyresygdomsprogression for nylig blevet forbundet med nedsat TFAM-aktivitet, hvilket resulterede i aktivering af fibrotiske og inflammatoriske veje på grund af mt-stress.14,24 I modsætning til seks2-Tfam-/-mutanter, mus med Ksp-Cre-medieret Tfam-inaktivering udviklede nyrefibrose og inflammation14, men ikke en cystisk sygdom. De fænotypiske forskelle mellem de 2 modeller er sandsynligvis en afspejling af, hvilke nyrecelletyper der var målrettet såvel som differentieringstilstanden af Cre-udtrykkende celler. Ksp-Cre medierer rekombination i det distale nefron med fremtrædende Cre-aktivitet i det medullære tykke ascenderende lem af Henle-segmentet og ureterisk knopafledt CD,25, hvorimod Six2-eGFP/Cre udtrykkes i cap-mesenchyme og ikke målretter mod ureteric knopafledte nefronsegmenter.16 I overensstemmelse med disse fund er stigningen i ekstracellulær matrixaflejring og fravær af cystisk sygdom hos 15-måned gamle Hoxb7-Tfam/mutanter; Hoxb7-Cre retter sig mod ureteriske knopafledte nefronsegmenter (Supplerende figur S5).26 I overensstemmelse med begrebet udviklingsstadie- og celletypeafhængighed er desuden observationen, at inaktivering af Tfam ved hjælp af Nphs{{16 }}Cre (Podocin-Cre) resulterede ikke i udviklingsmæssige eller voksne nyrefænotyper,27 hvorimod seks2-Tfam-/- mus udviklede betydelig albuminuri.

Acteosid iCistancheer god tilpolycystisk nyresygdom
Defekter i nefrondifferentiering var ikke helt uventede i seks2-Tfam-/- mus, fordi cellulær differentiering er blevet forbundet med øget afhængighed af OXPHOS til ATP-generering, hvorimod udifferentierede pluripotente celler foretrækker glykolyse frem for OXPHOS for at opfylde energibehovet.28 I hvilken grad bidrog det progressive tab af OXPHOS-aktivitet i sig selv til cystogenese hos seks{{1} }Tfam-/-mutanter kræver yderligere undersøgelse. Nylige undersøgelser har vist, at mutationer i PKD(polycystisk nyresygdom)1, som er ansvarlige for w85 procent af ADPKD-tilfælde,29 er forbundet med øget glykolytisk flux.30 Den patofysiologiske og terapeutiske betydning af dette fund er imidlertid ikke helt klar, fordi virkningerne af glucosemangel på cysteproliferation og PKD-progression er kontroversielle. 31,32.
Selvom vi ikke foreslår, at TFAM-dysfunktion repræsenterer en primær begivenhed i udviklingen af PKD(polycystisk nyresygdom), rejser vores undersøgelser muligheden for, at TFAM-dysfunktion kan have en medvirkende rolle i dets patogenese og/eller progression. Vi demonstrerer, at TFAM-proteinniveauer er reduceret i cysteforing af epitelceller fra murine og humane PKD-væv og fandt, at seks2-Tfam-/- væv deler molekylære træk med PKD(polycystisk nyresygdom)væv, der er forbundet med cystogenese. Unormal cilia-funktion er blevet impliceret i patogenesen af renale cystiske sygdomme.29,33,34 Selvom fraværet af cilia er blevet rapporteret for nogle PKD(polycystisk nyresygdom)dyremodeller,35,36 cilia dannes i Pkd1-/-epitelceller37 og blev også påvist i nyrecyster fra seks2-Tfam-/- mus (Supplerende figur S3). Adskillige signalveje forbundet med cystogenese er involveret i cilia-associeret signalering. Disse omfatter mitogenaktiveret proteinkinase/ekstracellulær signalreguleret kinasesignalering og b-catenin-regulerede veje.33 Både p-ERK- og b-catenin-niveauer var forhøjet i seks2-Tfam-/- nyrer, hvilket tyder på, at disse veje blev aktiveret. Disse fund er i overensstemmelse med observationer foretaget i humane ADPKD-celler og i flere murine PKD(polycystisk nyresygdom)modeller.38–43.
Peroxisomproliferator-aktiveret receptor-gamma coactivator 1a (PGC-1a), en opstrøms transkriptionel regulator af TFAM og driver af mt-biogenese, blev reduceret i cellelinjer isoleret fra patienter med ADPKD og ville, udover TFAM selv, repræsenterer et potentielt terapeutisk mål for PKD(polycystisk nyresygdom). En reduktion i PGC-1et udtryk er blevet foreslået for at fremme cysteproliferation på grund af øget mt-superoxidproduktion i PKD(polycystisk nyresygdom)1-defekte celler.44 Selvom vi ikke målte mt ROS-produktion i vores model, var vævsspecifik TFAM-inaktivering i andre celletyper forbundet med et fald og ikke en stigning i mt ROS-produktion.9 Ud over PGC -1a/TFAM-aksen har nyere undersøgelser fremhævet en potentiel rolle for hypoxi og den hypoxi-inducerbare faktor-vej i terapien af mt-sygdomme.45,46 I hvilken grad hypoxi-associerede veje kan udnyttes terapeutisk til behandlingen af sygdomme, der er forbundet med mt dysfunktion, såsom PKD, kræver yderligere undersøgelse.
Sammenfattende viser vores data, at mt-transkriptionsfaktor TFAM er nødvendig for normal nefrondifferentiering, og at tab af TFAM-aktivitet i nyreepitelceller reproducerer molekylære og metaboliske træk forbundet med PKD(polycystisk nyresygdom). Vores resultater giver et stærkt rationale for yderligere undersøgelser af mts sundhed og funktion i cystogenese. Vi foreslår, at terapeutiske strategier, der sigter mod at forbedre mt sundhed, kan være gavnlige for behandlingen af patienter med PKD(polycystisk nyresygdom).

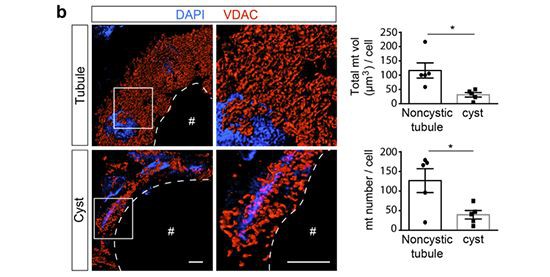
Figur 7|Mitokondriel transkriptionsfaktor A (TFAM) ekspression i nyrecyster fra patienter medpolycystisk nyresygdomer reduceret. (a) Repræsentative billeder af formalinfikserede paraffinindlejrede snit fra normale menneskelige nyrer og nyrer frapolycystisk nyresygdom(PKD) patienter analyseret ved immunhistokemi for TFAM-ekspression, ved immunofluorescens (IF) for spændingsafhængig anion-selektiv kanal 1 (VDAC) ekspression og ved RNA-fluorescerende in situ hybridisering for mitokondrielt kodet cytochrom c oxidase 1 (MT-CO1) og mitokondrielt kodet ATP-syntasemembranunderenhed 6 (MT-ATP6) mRNA-ekspression. Pile identificerer cysteforing af epitelceller, taltegn viser cystelumina, og stjerner viser glomeruli. Søjle =100 mm for billeder med lav forstørrelse og 10 mm for billeder med høj forstørrelse. (b) Repræsentative 3-dimensionelle strukturerede belysningsmikroskopiske billeder af menneskelig PKD (polycystisk nyresygdom)nyresnit analyseret med IF for VDAC-ekspression. 4', 6-diamidino-2-phenylindol (DAPI) blev brugt til nuklear farvning (blå fluorescens). Stiplede linjer markerer tubuli, og talskilte viser rørformet eller cyste lumina. Mitokondriel (mt) volumen blev kvantificeret ved hjælp af Imaris-software (n=5). Søjle=4 mm. Data er repræsenteret som gennemsnit plus -SEM og blev analyseret under anvendelse af Student's t-test. *P < 0.05.="" for="" at="" optimere="" visningen="" af="" dette="" billede,="" se="" venligst="" onlineversionen="" af="" denne="" artikel="" på="">

Cistancheer god tilpolycystisk nyresygdom
METODER
Genereringen af den betingede Tfam-allel er blevet beskrevet andetsteds.9 En detaljeret beskrivelse af muselinjer og eksperimentelle metoder kan findes i afsnittet Supplerende metoder og materialer. RNAseq-datasæt deles på geo@ncbi.nlm.hih.gov(adgangsnummer GSE147189).
Statistisk analyse
Data rapporteres som middel SEM. Statistiske analyser blev udført med Prism 6-software (GraphPad Software Inc., San Diego, CA) under anvendelse af Student's t-test. Overlevelse blev analyseret ved hjælp af Kaplan-Meier-metoden, og grupper blev sammenlignet med log-rank test. P-værdier på mindre end 0.05 blev betragtet som statistisk signifikante.
Studiegodkendelse
Alle procedurer, der involverede mus, blev udført i overensstemmelse med National Institutes of Healths retningslinjer for brug og pleje af levende dyr og blev godkendt af Vanderbilt University Institutional Animal Care and Use Committee.
AFSLØRING
Alle forfatterne erklærede ingen konkurrerende interesser.
ANKENDELSER
VHH støttes af Krick-Brooks-lærestolen i nefrologi ved Vanderbilt University, National Institutes of Health bevilger R01-DK101791 og R01-DK081646 og en Department of Veterans Affairs Merit Award 1I01BX002348. Yderligere støtte blev ydet af National Institutes of Health bevillinger R01-DK103033 (PVT), R01-DK108433 (MS) og R01-DK56942 (ABF); Vanderbilts O'BrienNyreCenter (P30-DK114809); Vanderbilt's Diabetes Research and Training Center (P30-DK20593); Digital Histology Shared Resource kerne på Vanderbilt University Medical Center (www.mc.vanderbilt.edu/dhsr); kernen Translational Pathology Shared Resource (P30-CA68485); Vanderbilt Mouse Metabolic Phenotyping Center (U24-DK059637); og Shared Instrumentation-bevillingen S10-OD023475. Oplysninger om arbejde udført i Haase-laboratoriet kan findes på www.haaselab.org.
FORFATTERS BIDRAG
VHH udtænkte projektet. KI, HK og VHH designede forskningsstudierne, analyserede og fortolkede data, skrev manuskriptet og lavede figurer. KI, HK, NG, KT, AL, CT, OD og CRB udførte eksperimenter og erhvervede og analyserede data. MS, NSC og PVT leverede musereagenser og musevæv og begrebsmæssig input og hjalp med fortolkningen af data. ABF og MEK leverede humane væv.

Cistancheer god tilpolycystisk nyresygdom
SUPPLERENDE MATERIALE
Supplerende fil (PDF)
Figur S1. Associeret med figur 1. Heterozygot Tfam-inaktivering i SIX2-progenitorceller associeres ikke mednyre sygdom. Der er vist repræsentative billeder af formalin-fikseret, paraffin-indlejretnyre sections from Cre littermate control and heterozygous Six2-Tfam β/ mice at (A) 3 months of age and (B) >10 months of age. Sections were stained with alcian blue/periodic acid–Schiff (AB-PAS) and analyzed by immunohistochemistry (IHC) for a smooth muscle actin (ACTA2) expression. Asterisks depict glomeruli. Bars ¼ 100 mm. Right panels show blood urea nitrogen (BUN) levels and renal mt DNA content in Cre littermate control and Six2-Tfamþ/mutant mice at 3 months of age (n ¼ 5 and 6, respectively) and age>10 måneder (henholdsvis n =4 og 3). Data er repræsenteret som gennemsnit 0,01. SEM og blev analyseret ved den 2-tailed Student's t-test; **P<>
Figur S2. Tilknyttet figur 1.Tfam-/- nyrecyster er afledt af celler med Six2-eGFP/Cre-ekspression. Der er vist repræsentative billeder af formalinfikserede, paraffinindlejrede nyresektioner fra seks2-mT/mG;Tfam-/-mus analyseret ved immunfluorescens (IF) med antistoffer mod det forstærkede grønne fluorescerende protein (eGFP) og tdTomat rødt fluorescerende protein. eGFP-ekspression indikerer seks2- eGFP/Cre-medieret rekombination af mT/mG Cre-reporter-allelen. (A) IF-analyse af tdTomat og/eller eGFP-ekspression inyreri alderen P7, P14 og P29. Stjerner viser store cyster afledt af seks2-eGFP/Cre-målrettede eGFP-udtrykkende celler (grøn fluorescens); taltegn viser 2 små cyster afledt af ikke-målrettede, tdTomatudtrykkende celler (rød fluorescens). Røde pile viser eGFP-negative celler (ingen rekombination). Hvide pile viser eGFP-positive cysteforingsceller (indikerer rekombination). Bar=100 mm. (B) Analyse af TFAM-udtryk ved hjælp af IF i Cre-kontrol og Six2-Tfam-/-mutanter i alderen P7. Hvide pile viser TFAM-positive rørformede strukturer (rød fluorescens). gl, glomerulus. Bar=25μm.
Figur S3. Tilknyttet figur 1.Tfam-/- nyrerer karakteriseret ved øget proliferativ aktivitet. (A) Repræsentative billeder af nyresektioner fra Cre kuldkammeratkontrol og Six2-Tfam-/-mus i alderen P14 blev analyseret for Ki67-ekspression ved immunhistokemi (IHC). Røde pile viser Ki67-positive celler i kontrol ogTfam-/- nyres. Søjle =100 mm. (B) Immunoblotanalyse af ERK, phospho-ERK (p-ERK) og b-catenin ekspression i sin helhednyrehomogenater fra Cre kuldkammeratkontrol og seks2- Tfam/mutante mus i alderen P14. (C) Spaltet caspase 3 udtryk i formalinfikseret, paraffinindlejretnyresektioner fra Cre littermate control og Six2-mT/mG;Tfam-/- mus i alderen P14 analyseret af IHC. Røde prikker blev placeret over spaltede caspase 3-positive celler for at illustrere vævsfordeling ved lav-effekt forstørrelse. Røde pile viser spaltede caspase 3-positive celler i højeffekts forstørrelsesbilleder. Stænger =1 mm (øverst) og 100 mm (bund). (D) Cilial axoneme-mærkning ved immunfluorescens med anti-acetyleret a-tubulinfarvning. Der er vist repræsentative billeder af formalin-fikseret, paraffin-indlejretnyresektioner fra Cre littermate control og Six2-Tfam-/- mutante mus i alderen P14. #, ##, ### viser henholdsvis små, mellemstore og store cyster. Hvide pile viser cilia. Stænger =100 mm (øverst) og 10 mm (bund).
Figur S4. Associeret med figur 2. Inaktivering af Tfam i SIX2-afstamning inhiberer nefronmodning. Der er vist repræsentative billeder af formalin-fikseret, paraffin-indlejretnyresektioner fra Cre littermate control og Six2-Tfam-/- mutante mus i alderen P{{{{10}}}}, P7 og P14 (n=4–6). Sektionen blev analyseret ved lectinhistokemi under anvendelse af lotus tetragonolobus (LTL) lectin og Dolichos biflorus agglutinin (DBA) lectin. Wilms tumor 1 (WT1) proteinekspression blev analyseret ved immunfluorescens. Områder med LTL- og DBA-tubuli blev kvantificeret med ImageJ (National Institutes of Health, Bethesda, MD); antallet af glomeruli blev talt manuelt. Hvide pile viser nefroner, der reagerer med LTL eller DBA, og asterisker viser glomeruli. Stænger ¼ 100 mm. Data er repræsenteret som gennemsnitlig SEM og blev analyseret ved en 2-tailed Student's t-test. **P < 0,01.="" ***p=""><>

Cistancheer god tilpolycystisk nyresygdom
Figur S5. Associeret med figur 2. Inaktivering af Tfam i HOXB7 progenitorceller resulterer ikke i cysteudvikling. (A) Der er vist repræsentative billeder af formalinfikseret, paraffinindlejretnyreafsnit fra 3-måned gammel heterozygot Hoxb7-Tfamþ/ og Hoxb7-Tfam-/- mutante mus. Sektioner blev farvet med Masson trichrome (MTrichrome) og analyseret ved immunfluorescens (IF) for tdTomat (TDT) og cytochromoxidase IV (COX IV) ekspression. Nummerskilte viser udvidede tubuli i MTrichrome-farvede sektioner, og asterisker viser tdT-positive HOXB7 progenitorcelle-afledte opsamlingskanaler. (B) IF og RNA fluorescerende in situ hybridisering (RNA-FISH) billeder af formalinfikserede, paraffinindlejrede nyresektioner fra 3-måned gammel heterozygot Hoxb7-Tfam-/-og Hoxb7-Tfam-/- mutante mus. Sektioner blev analyseret for tdT- og AQP2-proteinekspression med IF- og tdT-RNA og mitokondrielt kodet cytochrom c-oxidase-underenhed 1 (mt-Co1) RNA-ekspression af RNA-FISH. Stjerner viser TD-udtrykkende tubuli (samlekanaler). I Hoxb7-Tfam-/- mutante mus tdT-udtrykkende tubuli udtrykker ikke AQP2 og mt-Co1. Søjle =100 mm. (C) Repræsentative billeder afnyresektioner fra 15-måned gammel kontrol og Hoxb7-Tfam-/-mus farvet med MTrichrome. Søjle =100 mm. Højre panel, blodurinstofnitrogen (BUN) fra Cre kuldkammerat kontrolmus og Hoxb7-Tfam-/- mutanter (n=6 hver). Data er repræsenteret som gennemsnitlig SEM og blev analyseret ved hjælp af en 2-tailed Student's t-test.
Figur S6. Associeret med figur 3. Mangel på nefronsegmentmarkørekspression i cyster fra seks2-Tfam-/- nyrer. Repræsentative billeder af formalin-fikseret, paraffin-indlejretnyresektioner fra seks2-mT/mG;Tfam-/- mus i en alder af P14. Sektioner blev analyseret ved immunfluorescens med antistoffer, der er specifikke for forstærket grønt fluorescerende protein (eGFP), megalin, uromodulin, thiazidfølsom natriumchlorid-cotransporter (NCC) og aquaporin 2 (AQP2). Sammenlagte billeder vises til højre. Pile angiver rørformede strukturer, der udtrykker de respektive nefronsegmentmarkører. Bar=100μm.
Figur S7. Tilknyttet figur 4.Hold-/- epitelceller mangler MT-CO1. (A) Der er vist repræsentative billeder af formalinfikseret, paraffinindlejretnyresektioner fra seks2-mT/mG;Tfam-/- mus i en alder af P7. Nyresektioner blev analyseret ved immunfluorescens for ekspression af forstærket grønt fluorescerende protein (eGFP) og mitokondrielt kodet cytochrom c oxidase underenhed 1 (MT-CO1). eGFP-ekspression indikerer seks2-eGFP/Cre-medieret rekombination af mT/mG Cre-reporter-allelen. Stjerner viser eGFP-negative tubuli (ingen rekombination), som udtrykker MT-CO1; taltegn viser eGFP-positive tubuli (rekombineret), som ikke udtrykker MT-CO1, hvilket indikerer tab af TFAM-funktion. Bar =100μm.
Figur S8. Associeret med figur 5. Inaktivering af Tfam i SIX2-afstamningsceller ændrer ekspressionen af metaboliske gener. Genom-dækkende RNA-ekspressionsanalyse af RNAseq blev udført med hele nyrebarken isoleret fra Cre kontrol kuldkammerat og Six2-Tfam-/- mutante mus i alderen P7. Der vises varmekort, der illustrerer ændringer i ekspressionsmønstrene for gener involveret i oxidativ fosforylering, glykolyse, glukosetransport, fedtsyremetabolisme og tricarboxylsyrecyklussen (n=4 hver).
Figur S9. Associeret med figur 6. TFAM-ekspression er reduceret i Cyscpk/cpk-nyrecyster. (A) Der er vist repræsentative billeder af formalinfikserede, paraffinindlejrede nyresektioner fra Cyscpk/cpkmus i en alder af P18. Sektioner blev analyseret ved RNA fluorescerende in situ hybridisering for mitokondrielt kodet cytochrom c oxidase subunit 1 (mt-Co1) og mitokondrielt kodet ATP syntase membran subunit 6 (mt-Atp6) ekspression, ved immunofluorescens (IF) for spændingsafhængig kanal anion-selektiv 1 (VDAC) ekspression og ved lectinhistokemi med lotus tetragonolobus lectin (LTL). Hvide pile viser cystebeklædning af epitelceller, stiplede linjer angiver cystebeklædning af epitelceller, og talskilte viser cystelumina. Stænger ¼ 100 mm (laveffektforstørrelse) og 10 mm (højeffektforstørrelse). (B) 3D struktureret belysningsmikroskopi (3D SIM) af kuldkammerat vildtypenyrei en alder af P18. Der er vist repræsentative billeder af nyresektioner farvet med LTL og analyseret med IF for cytochrom c-oxidase-underenhed IV (COX IV) og VDAC-ekspression. Søjle ¼ 10 mm (laveffekt forstørrelsesbilleder) og 2 mm (højeffekt forstørrelsesbilleder). Asterisk viser en interstitiel cellekerne.
Figur S10. Associeret med figur 7. TFAM-ekspression er nedsat i nyrecyster fra patienter medpolycystisk nyresygdom. Relative TFAM-ekspressionsniveauer i nyrecyster fra 5 patienter medpolycystisk nyresygdomblev vurderet ved immunhistokemi (n=5). Vist er andelen af cyster med lav eller høj TFAM-ekspression i cysteforingsepitel. Antallet af talte cyster pr. sektion er vist med hvidt.

Cistancheprodukter er gode tilpolycystisk nyresygdom
Uddrag fra: 'Nyreepitel-målrettet mitokondriel transkriptionsfaktor A-mangel resulterer i progressiv mitokondriel udtømning forbundet med alvorlig cystisk sygdom' af Ken Ishii1,2,11 et al.
---NyreInternational (2021) 99, 657-670
REFERENCER
1. West AP, Shadel GS. Mitokondrielt DNA i medfødte immunresponser og inflammatorisk patologi. Nat Rev Immunol. 2017;17:363-375.
2. Chandel NS. Udvikling af mitokondrier som signalorganeller. Celle Metab. 2015;22:204–206.
3. Campbell CT, Kolesar JE, Kaufman BA. Mitokondriel transkriptionsfaktor A regulerer mitokondriel transkriptionsinitiering, DNA-pakning og genomkopinummer. Biochim Biophys Acta. 2012;1819:921-929.
4. Kukat C, Larsson NG. mtDNA laver en u-vending for mitokondrienukleoidet. Trends Cell Biol. 2013;23:457-463.
5. Taanman JW. Det mitokondrielle genom: struktur, transkription, translation og replikation. Biochim Biophys Acta. 1999;1410:103-123.
6. Larsson NG, Wang J, Wilhelmsson H, et al. Mitokondriel transkriptionsfaktor A er nødvendig for mtDNA-vedligeholdelse og embryogenese hos mus. Nat Genet. 1998;18:231-236.
7. Larsson NG, Rustin P. Dyremodeller for respiratorisk kædesygdom. Trends Mol Med. 2001;7:578-581.
8. Torraco A, Diaz F, Vempati UD, et al. Musemodeller af oxidative phosphoryleringsdefekter: kraftfulde værktøjer til at studere patobiologien af mitokondrielle sygdomme. Biochim Biophys Acta. 2009;1793:171-180.
9. Hamanaka RB, Glasauer A, Hoover P, et al. Mitokondrielle reaktive oxygenarter fremmer epidermal differentiering og udvikling af hårsækkene. Sci signal. 2013;6:ra8.
10. Vernochet C, Mourier A, Bezy O, et al. Adipose-specifik deletion af TFAM øger mitokondriel oxidation og beskytter mus mod fedme og insulinresistens. Celle Metab. 2012;16:765-776.
11. Hall AM, Unwin RJ, Hanna MG, et al. Nyrefunktion og mitokondriel cytopati (MC): flere spørgsmål end svar? QJM. 2008;101:755-766.
12. Emma F, Montini G, Parikh SM, et al. Mitokondriel dysfunktion ved arvelig nyresygdom og akut nyreskade. Nat Rev Nephrol. 2016;12: 267-280.
13. Kang I, Chu CT, Kaufman BA. Den mitokondrielle transkriptionsfaktor TFAM i neurodegeneration: nye beviser og mekanismer. FEBS Lett. 2018;592:793 811.
14. Chung KW, Dhillon P, Huang S, et al. Mitokondriel skade og aktivering af STING-vejen fører til nyrebetændelse og fibrose. Celle Metab. 2019;30:784–799.e785.
15. Lille MH, McMahon AP. Pattedyrs nyreudvikling: principper, fremskridt og fremskrivninger. Cold Spring Harb Perspect Biol. 2012;4:a008300.
16. Kobayashi A, Valerius MT, Mugford JW, et al. Six2 definerer og regulerer en multipotent selvfornyende nefron-progenitor-population gennem pattedyrs nyreudvikling. Celle stamcelle. 2008;3:169-181.
17. Wredenberg A, Wibom R, Wilhelmsson H, et al. Øget mitokondriel masse i mitokondriel myopati mus. Proc Natl Acad Sci US A. 2002;99:15066–15071.
18. Guder WG, Ross BD. Enzymfordeling langs nefronen. Nyre Int.1984;26:101–111.
19. Guery B, Choukroun G, Noel LH, et al. Spektret af systemisk involvering hos voksne med nyrelæsion og mitokondriel tRNA(Leu) genmutation. J Am Soc Nephrol. 2003;14:2099-2108.
20. O'Toole JF, Liu Y, Davis EE, et al. Personer med mutationer i XPNPEP3, som koder for et mitokondrielt protein, udvikler nefronophthisis-lignende nefropati. J Clin Invest. 2010;120:791-802.
21. Alston CL, Morak M, Reid C, et al. En ny mitokondriel MTND5-rammeskiftmutation, der forårsager isoleret kompleks I-mangel, nyresvigt og myopati. Neuromuskulær lidelse. 2010;20:131-135.
22. Finsterer J, Scorza FA. Nyremanifestationer af primære mitokondrielle lidelser. Biomed Rep. 2017;6:487-494.
23. Fervenza FC, Gavrilova RH, Nasr SH, et al. CKD på grund af en ny mitokondriel DNA-mutation: en sagsrapport. Am J Nyre Dis. 2019;73:273-277.
24. Huang S, Park J, Qiu C, et al. Jagged1/Notch2 kontrollerer nyrefibrose via Tfam-medieret metabolisk omprogrammering. PLoS Biol. 2018;16:e2005233.
25. Shao X, Somlo S, Igarashi P. Epitelspecifik Cre/lox-rekombination i den udviklende nyre og genitourinary-kanal. J Am Soc Nephrol.2002;13:1837–1846.
26. Yu J, Carroll TJ, McMahon AP. Sonic hedgehog regulerer proliferation og differentiering af mesenkymale celler i musens metanephric nyre. Udvikling. 2002;129:5301-5312.
27. Brinkkoetter PT, Bork T, Salou S, et al. Anaerob glykolyse opretholder den glomerulære filtrationsbarriere uafhængig af mitokondriel metabolisme og dynamik. Cell Rep. 2019;27:1551–1566.e1555.
28. Wanet A, Arnould T, Najimi M, et al. Forbind mitokondrier, stofskifte og stamcelleskæbne. Stamceller Dev. 2015;24:1957-1971.
29. Guay-Woodford LM. Nyrecystiske sygdomme: forskellige fænotyper konvergerer på cilium/centrosomkomplekset. Børnelæge Nephrol. 2006;21:1369-1376.
30. Rowe I, Chiaravalli M, Mannella V, et al. Defekt glukosemetabolisme ved polycystisk nyresygdom identificerer en ny terapeutisk strategi. Nat Med.2013;19:488–493.
31. Warner G, Hein KZ, Nin V, et al. Fødevarebegrænsning forbedrer udviklingen af polycystisk nyresygdom. J Am Soc Nephrol. 2016;27:1437-1447.
32. Chiaravalli M, Rowe I, Mannella V, et al. 2-Deoxy-d-glucose forbedrer PKD(polycystisk nyresygdom)progression. J Am Soc Nephrol. 2016;27:1958-1969.
33. Hildebrandt F, Benzing T, Katsanis N. Ciliopathies. N Engl J Med. 2011;364: 1533-1543.
34. Harris PC, Torres VE. Genetiske mekanismer og signalveje i autosomal dominant polycystisk nyresygdom. J Clin Invest. 2014;124:2315-2324.
35. Pazour GJ, Dickert BL, Vucica Y, et al. Chlamydomonas IFT88 og dets musehomolog, polycystisk nyresygdomsgen tg737, er påkrævet til samling af cilia og flageller. J Cell Biol. 2000;151:709-718.
36. Lin F, Hiesberger T, Cordes K, et al. Nyrespecifik inaktivering af underenheden af kinesin-II hæmmer renal ciliogenese og producerer polycystisk nyresygdom. Proc Natl Acad Sci US A. 2003;100:5286–5291.
37. Nauli SM, Alenghat FJ, Luo Y, et al. Polycystin 1 og 2 medierer mekanosensation i nyrecellernes primære cilium. Nat Genet. 2003;33:129-137.
38. Saadi-Kheddouci S, Berrebi D, Romagnolo B, et al. Tidlig udvikling af polycystisk nyresygdom hos transgene mus, der udtrykker en aktiveret mutant af beta-cateningenet. Onkogen. 2001;20:5972-5981.
39. Yamaguchi T, Nagao S, Wallace DP, et al. Cyklisk AMP aktiverer B-Raf og ERK i cysteepitelceller fra autosomal-dominante polycystiske nyrer. Nyre Int. 2003;63:1983-1994.
40. Nagao S, Yamaguchi T, Kusaka M, et al. Nyreaktivering af ekstracellulær signalreguleret kinase hos rotter med autosomal-dominant polycystisk nyresygdom. Nyre Int. 2003;63:427-437.
41. Qian CN, Knol J, Igarashi P, et al. Cystisk nyre-neoplasi efter betinget inaktivering af APC i musenyretubulært epitel. J Biol Chem. 2005;280:3938-3945.
42. Omori S, Hida M, Fujita H, et al. Ekstracellulær signalreguleret kinasehæmning bremser sygdomsprogression hos mus med polycystisk nyresygdom. J Am Soc Nephrol. 2006;17:1604-1614.
43. Shibazaki S, Yu Z, Nishio S, et al. Cystedannelse og aktivering af den ekstracellulære regulerede kinasevej efter nyrespecifik inaktivering af PKD(polycystisk nyresygdom)1. Hum Mol Genet. 2008;17:1505-1516.
44. Ishimoto Y, Inagi R, Yoshihara D, et al. Mitokondriel abnormitet letter cystedannelse ved autosomal dominant polycystisk nyresygdom. Mol Cell Biol. 2017;37:e00337-17.
45. Jain IH, Zazzeron L, Goli R, et al. Hypoxi som terapi for mitokondriesygdom. Videnskab. 2016;352:54–61.
46. Ferrari M, Jain IH, Goldberger O, et al. Hypoxibehandling reverserer neurodegenerativ sygdom i en musemodel af Leigh syndrom. Proc Natl Acad Sci US A. 2017;114:E4241–E4250.
