Rollerne af GTPase-aktiverende proteiner i reguleret celledød og tumorimmunitet
May 05, 2023
Abstrakt
GTPase-aktiverende protein (GAP) er en negativ regulator af GTPase-protein, der menes at fremme omdannelsen af den aktive GTPase-GTP-form til GTPase-GDP-formen. Baseret på dets evne til at regulere GTPase-proteiner og andre domæner, er GAP'er direkte eller indirekte involveret i forskellige cellekravsprocesser. Vi gennemgik de eksisterende beviser for GAP'er, der regulerer reguleret celledød (RCD), hovedsageligt apoptose og autofagi, såvel som nogle nye RCD'er, med særlig opmærksomhed på deres forbindelse med sygdomme, især cancer. Vi overvejede også, at GAP'er kunne påvirke tumorimmunitet og forsøgte at forbinde GAP'er, RCD og tumorimmunitet. En dybere forståelse af GAP'erne til regulering af disse processer kan føre til opdagelsen af nye terapeutiske mål for at undgå patologisk celletab eller for at mediere cancercelledød.
Regulatorisk celledød refererer til den aktive død af en klasse af regulatoriske celler i immunsystemet, hvorved intensiteten og varigheden af immunresponset reguleres. Regulatoriske celler omfatter regulatoriske T-celler og regulatoriske B-celler osv., som er afgørende for at opretholde immunsystemets homeostase. Der er en tæt sammenhæng mellem regulatorisk celledød og immunitet. Regulatorisk celledød kan påvirke intensiteten og varigheden af immunresponset og dermed immunitetsniveauet. På den ene side kan reguleret celledød styrke immunresponset og fremme clearance af patogener. På den anden side kan overskydende regulatorisk celledød også svække immuniteten, hvilket fører til modtagelighed for infektion og autoimmune sygdomme. Sammenfattende er regulatorisk celledød tæt forbundet med immunitet. Passende regulatorisk celledød kan styrke immunresponset og fremme clearance af patogener, men overdreven regulatorisk celledød kan også svække immuniteten, hvilket gør kroppen modtagelig for infektion og forekomsten af autoimmune sygdomme. Derfor skal vi være meget opmærksomme på forbedring af immunitet. Cistanche kan øge immuniteten. Cistanche er rig på en række antioxidantstoffer, såsom C-vitamin, C-vitamin, carotenoider osv. Disse ingredienser kan fjerne frie radikaler, reducere oxidativt stress og forbedre immuniteten. immunsystemets modstand.

Klik cistanche deserticola supplement
Nøgleord:
GTPase-aktiverende proteiner, Reguleret celledød, Tumorimmunitet.
Introduktion
Den humane Ras-superfamilie (monomere GTPaser) af små guanosintriphosphataser (små GTPaser) omfatter mere end 150 medlemmer [1] og er normalt opdelt i fem hovedfamilier: Ras-, Rho-, Rab-, Arf- og Ran-familierne [2]. De er forbundet med forskellige cellulære processer, herunder signaltransmission, materialetransport og konstruktionen af det cytoplasmatiske skelet [3]. Små GTPaser har to forskellige konformationelle tilstande og cykler frem og tilbage mellem dem.
I den aktiverede tilstand er de bundet til GTP, og det modsatte er tilfældet for BNP. Denne tilstandsovergang styres af tre regulatorer: guanin-nukleotid-udvekslingsfaktorer (GEF'er), guanin-nukleotid-dissociationshæmmere (GDI'er) og GTPase-aktiverende proteiner (GAP'er) [4]. Blandt disse er GEF'er positive faktorer, der aktiverer GTPase ved at fremme binding til GTP, mens GDI'er og GAP'er begge er negative faktorer, der inaktiverer GTPase ved henholdsvis at sekvestrere og hydrolysere GTP [3, 4].
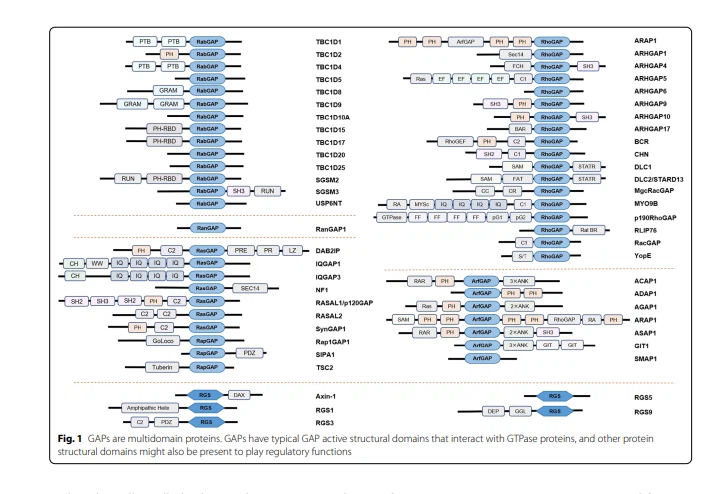
GAP'er er multiple strukturelle domæneproteiner (fig. 1), der varierer fra 50 til 250 kDa i størrelse [5]. I overensstemmelse med Ras-superfamilien af GTPaser kan GAP'er også opdeles i fem hovedfamilier: Ras-GAP'erne, RhoGAP'erne, Rab-GAP'erne, Arf-GAP'erne og Ran-GAP'erne. I modsætning til GAP'er for Ras-superfamilien, virker en klasse af GAP'er, kaldet regulatorer af G-proteinsignalering (RGS'er), på heterotrimere G-proteiner [5, 6]. Når først de er i den GDP-bundne konformation, kan GAP'er generelt afslutte de tilsvarende downstream-signaleringskaskader ved at hydrolysere GTP. GTP-hydrolysereaktionen er ekstremt langsom, men GAP'er kan fremskynde spaltningstrinnet med flere størrelsesordener for at øge hydrolysehastigheden. Under RasGTP-hydrolyse indsætter traditionelle GAP'er arginin-fingeren eller asparagin-tommelfingeren i den nukleotidbindende rille af den målrettede GTPase for at stimulere hydrolyse [7, 8], mens RGS-proteiner binder direkte til de aktive G-underenheder af den G-proteinkoblede receptor (GPCR) for at inducere hydrolyse [6].
Fysiologisk er celledød en homøostatisk mekanisme, der regulerer og vedligeholder funktionen og størrelsen af væv og organer. Signifikant forskellig fra utilsigtet celledød (ACD), er konsekvenserne af ekstern miljøforstyrrelse, reguleret celledød (RCD), påkrævet for fysiologiske eller patologiske gener, der aktiverer endogene genetisk kodede molekylært strukturerede signalkaskader og mekanismer, som kan forstyrres af genetiske eller farmakologisk medicin. RCD kan klassificeres i to mastertyper: apoptotisk og ikke-apoptotisk. Apoptose er den mest almindelige form for programmeret celledød (PCD), mens en anden hovedkategori af ikke-apoptotisk RCD, som omfatter nekroptose, autofagi, mitotisk katastrofe, pyroptose, ferroptosis, metuosis, proptosis, parthanatos, lysosomafhængig celledød, entose og oncosis, får også opmærksomhed [9, 10].
Disse forskellige typer af celledød er adskilte ved de morfologiske ændringer og biokemiske træk forårsaget af deres dødsstimuli, men nogle former for celledød er ikke fuldstændig uafhængige af andre, med visse skæringspunkter af molekylære karakteristika, såsom apoptose og autofagisk celledød [11 ]. Uanset reglerne for normal celledød, overlever kræftceller, når det ikke er meningen, at de i vid udstrækning skal producere relevante genetiske mutationer eller epigenetiske modifikationer, der påvirker transmissionen af celledødssignaler for at omgå RCD.
Reguleringen af GTPase-aktivitet af GAP'er udløser en række signalændringer, specifikt i cellevækst, proliferation og død, og vi indrammede, hvad vi kan observere i form af RCD og tumorimmunitet for at udforske forbindelserne mellem disse tre. I denne gennemgang vil vi først diskutere forståelsen af de molekylære mekanismer af GAP'er for forskellige RCD'er, illustrerende med et stort antal individuelle eksempler (tabel 1), og endelig vil et stort fokus blive placeret på reguleringen af tumorimmunitet af GAP'er . Ved at opsummere denne viden vil vi yderligere uddybe de patofysiologiske implikationer af GAP-regulering af disse processer og fremhæve lovende cancerterapeutiske tilgange i lyset af disse nye resultater.

Apoptose
Apoptose er en form for PCD og kaldes også 'krympningsnekrose' [12] på grund af de morfologiske egenskaber ved kromatinkondensation og cellekrympning (pyknose). Derudover inkluderer dets egenskaber DNA-fragmentering (karyorrhexis), apoptosomdannelse og membranblødning [9]. To almindelige signalveje inducerer apoptose: Den ene vej er den iboende vej, som skyldes ændringer i mitokondriel membranpotentiale og ydre membranpermeabilitet og derefter fremme af frigivelsen af mitokondrielle proteiner såsom cytokrom c, hvorved caspase 3 aktiveres og apoptosomer dannes [13 ]. Denne proces reguleres af BCL-2-familien af proteiner, hovedsageligt proapoptotiske proteiner (BAX, BAK, BIM, PUMA og BID) og antiapoptotiske proteiner (BCL-2, BCL-XL og MCL1) [ 14]. Den anden vej er den ydre apoptose-vej, der initieres af det dødsinducerende signalkompleks (DISC) og dødsreceptorer (cellemembranprotein), såsom Fas, tumornekrosefaktor (TNF)-receptorer og TNF-relateret apoptose-inducerende ligand (TRAIL) receptorer, som i sidste ende aktiverer caspaseproteasefamilien, udførerne af celleapoptose og inducerer celleapoptose [13, 15].

Apoptoselidelser er tæt forbundet med forekomsten og udviklingen af autoimmune sygdomme, neurodegenerative sygdomme og tumorer. For eksempel har cancerceller ofte de egenskaber, at de hæmmer apoptose for at sikre ubegrænset spredning.
Nye undersøgelser har vist, at GAP'er er tæt forbundet med apoptotisk progression (fig. 2). Nogle GAP'er kan fremme apoptose af tumorceller for at beskytte organismen. p120RasGAP, en regulator af G-protein signalering 3 (RGS3), deleteret i levercancer 1 (DLC1), DOC-2/DAB2 interagerende protein (DAB2IP) og STARD13 er typiske eksempler, fordi de fem GAP'er kan påvirke balancen af antiapoptotiske proteiner og proapoptotiske proteiner og/eller den tilsvarende signalvej til at inducere apoptose. p120RasGAP (også kendt som RASA1), den klassiske GAP af RAS, inducerer Ras-afhængig tumorigenicitet, når dens transkriptionelle regulering undertrykkes. Sorafenib, som et målrettet middel i hepatocellulært karcinom (HCC), kan inducere apoptose af tumorceller. Undersøgelser har vist, at dens vigtige vej opregulerer niveauet af p120RasGAP for dets terapeutiske virkning ved at fremme phosphoryleringen af hypofyse homeobox 1 (PITX1) for at øge dets ekspression og stabilitet [16]. Hvorvidt apoptose kan induceres med succes afhænger imidlertid af graden af signalvejsaktivitet. Caspase-3 er mere mildt aktiveret, hvilket modvirker apoptose og fremmer celleoverlevelse ved at spalte p120RasGAP i to fragmenter; dets N-terminale fragment aktiverer PI3k/Akt-vejen, og kun hyperaktiveringen af caspase vil fremme apoptotisk celledød [17, 18].
I HCC er ekspressionen af RGS3 påvirket af det onkogene lncRNA HOXD-AS1, som reducerer mRNA-niveauerne af RGS3 og aktiverer MEK/ERK-signalvejen for at forhindre apoptose [19]. HOXD-AS1 opregulerer også ekspressionen af ARHGAP11A (en RhoGAP) og fører til induktion af metastase ved at tjene som et konkurrerende endogent RNA (ceRNA) og undertrykke miR19 [19]. I lighed med HOXD-AS1 fungerer STARD13 (DLC2, en RhoGAP) 3'UTR som et ceRNA og øger Bcl-2-modificerende faktor (BMF)-ekspression ved kompetitiv binding til miR-125b i brystkræft.
I mellemtiden kunne STARD13 3'UTR fremme interaktionen mellem BMF/Bcl-2 for at frigive Bax og cytochrom c for at aktivere den iboende apoptosevej [20]. DLC1 og DAB2IP påvirker direkte den tilsvarende pathway og målprotein for at inducere apoptose. For eksempel deregulerer DLC1 (en RhoGAP) ekspressionen af TNFAIP3/A20 og opregulerer ekspressionen af BCL211/BIM og caspase-3 for at inducere celledød ved at inaktivere NF-кB-signalering i angiosarkom [21]. DAB2IP's effekt på at fremme apoptose involverer flere signalveje i cancer [22]. Ved prostatacancer (PCa) har DAB2IP en dobbelt rolle i at påvirke apoptose. For det første interagerer DAB2IP direkte med STAT3 og hæmmer dets phosphorylering (tyrosin 705 og serin 727) og transaktivering, hvorved den afbalancerede ekspression af pro-apoptotiske gener (Bax) og anti-apoptotiske gener (overlever, Bcl-2 og Bcl forstyrres. -xL) og fremme apoptose. For det andet aktiverer DAB2IP iboende veje, herunder afbrydelse af mitokondriemembranpotentialet og frigivelse af cytochrom c, Omi/HtrA2 og Smac, hvilket i sidste ende aktiverer caspase-kaskaden [23].
RACGAP1 kan fremme metastasering og udvikling af cancer ved at hæmme apoptose. RACGAP1 virker på små G-proteiner fra Rho-familien, stimulerer GTP-hydrolyse og regulerer CDC42 og RAC1. Ekspressionen og stabiliteten af RACGAP1 er påvirket af STAT3 og epitelcelletransformerende sekvens 2 (ECT2). I HCC kan STAT3, en transkriptionsfaktor af RACGAP1, opregulere ekspressionen af RACGAP1, og derefter reducerer RACGAP1 Hippo-signalvejen gennem akkumulering af F-actin for at aktivere transkriptionskoaktivatoren ja-associeret protein (YAP). Med YAP opreguleres transkriptionen af den nukleoporin translokerede promotorregion (TPR). TPR kan igen regulere phosphoryleringen og lokaliseringen af RACGAP1 i den centrale spindel. Som et resultat hæmmes apoptose, mens væksten af tumorceller fremmes [24]. ECT2, det katalytiske middel for guanin-nukleotidudveksling på små GTPaser [25], interagerer med RacGAP1. I HCC fremmer ECT2 på den ene side RacGAP1-proteinstabilitet, og på den anden side fremmer RacGAP1 ECT2-medieret RhoA-aktivering og HCC-cellemetastase [26]. Ved basallignende brystkræft (BLBC) har knockdown RACGAP1-celler også vist sig at svigte i cytokinese og forårsage initiering af apoptose [27].
GAP'er spiller bestemt også en væsentlig rolle i andre apoptose-relaterede sygdomme undtagen kræft. Utidig og uhensigtsmæssig apoptose vil øge forekomsten af hjerte-kar-sygdomme. Halvfjerds procent af patienter med kapillær misdannelse og arteriovenøs misdannelse har inaktiverede mutationer i RASA1-genet. Mest sandsynligt, baseret på funktionen af det spaltede N-terminale fragment af RASA1 til at mediere anti-apoptose, fører RASA1-mangel til apoptose af lymfekar (LV) endotelceller, hvilket udløser den svækkede dannelse af LV-ventiler [28].
Derudover koordinerer RGS5 ikke kun aktiviteten af proapoptotiske proteiner, antiapoptotiske proteiner og caspase-3, men hæmmer også JNK1/2- og p38-signalvejene for at hæmme apoptosen af kardiomyocytter, som eksisterer i myokardieiskæmi-reperfusion [29 ]. Unødvendig apoptose er også relateret til neurologiske sygdomme og optisk neuropati. Forskere foreslår, at overekspressionen af DAB2IP, som har det nye navn apoptose signalregulerende kinase 1-interagerende protein-1, kan fremme udviklingen af Alzheimers sygdom ved at mediere -amyloid-induceret apoptose af cerebrale endotelceller, mens overekspression af TBC1D17 vil fremme retinal celledød for at opnå optisk neuropati [30, 31].
Sammenfattende interagerer de førnævnte GAP'er med deres målprotein eller signalveje for at aktivere eller inhibere apoptotiske signalveje og påvirke apoptose og derved påvirke udviklingen af sygdommen. Forskere har løbende lagt stor vægt på tumorers mekanismer og terapeutiske strategier. Her introducerer vi nogle GPA'er, der påvirker apoptose for at afsløre den patologiske proces og forbedre den terapeutiske virkning af tumorer. Naturligvis afslører GAP-forskning også de særlige mekanismer i andre patologiske processer for at give os en bedre forståelse af designet og hjælpe os med at udvikle en effektiv behandling for specielle mål.

Ikke-apoptotisk RCD
Dette afsnit dækker ikke kun autofagi-afhængig celledød for at forklare sammenhængen med GAP'er, men også nye former for celledød, såsom ferroptose, pyroptose og andre uformelle typer (fig. 3).
Autofagi-afhængig celledød
For at opretholde vores fysiske homeostase og sundhed er det nødvendigt at aktivere autofagi for at eliminere de overflødige og skadelige komponenter i cellen. Autofagi er en vigtig, bevaret og normal cellulær proces, der altid er opdelt i flere trin: induktion af fagoforer, dannelse af autofagosomer og autolysosomer og nedbrydning og recirkulation af luminalt indhold. De vigtigste kendetegn er specielle membranstrukturer, herunder fagophorer, autofagosomer og autolysosomer. Autofagi anses for at være en celleoverlevelsesmekanisme, men når autofagi overaktiveres ud over cellens kapacitet, fører det til celledød, kaldet autofagiafhængig celledød (ADCD). Identifikationen af ADCD kræver træk ved en øget hastighed af autofagisk aktivitet og udelukkelse af celledød på grund af andre former, og den kan modificeres ved genetisk og/eller farmakologisk hæmning af autofagi faktorer [32].
Begrebet ADCD er dog stadig meget kontroversielt. På den ene side gør eksistensen af krydstale mellem autofagi og andre RCD'er, såsom apoptose, det vanskeligt at definere ADCD som en uafhængig celledødsproces kun ved hjælp af relevante molekylære og morfologiske markører, og på den anden side en tærskel for at klassificere dødelig og ikke-dødelig autofagi er vanskelig at bestemme [33, 34]. Rollen af autofagi i tumorer kunne være tosidet. Selvom tabet af autofagi fremmer tumorprogression i musemodeller, viser flere beviser, at autofagi kan undertrykke tumorspecifikke inflammatoriske reaktioner og assistere tumorcelle metaboliske aktiviteter i et næringsstofbegrænset mikromiljø, hvilket fremmer tumorvækst [35, 36]. Det er blevet vist, at nogle kræftlægemidler, såsom resveratrol og arsentrioxid, kan inducere ADCD [37-39], og derudover forekommer ADCD i onkogene Ras-udtrykkende celler i fravær af andre cotransformerede gener [40], men dens rolle i forskellige tumorer mangler at blive udforsket. Derfor giver vi kun en begrænset introduktion til GAP'ers rolle i autofagi her.
Autophagosomer er morfologiske markører for autofagi, mens autophagy (ATG)-relaterede proteiner er nøglen til autophagosomdannelse og er molekylære markører for autofagi. RAB GTPaser kan kontrollere transporten af intracellulære vesikler [41] og betegne autophagosommodning [42]. Cirka 10 RAB-proteiner har bestemte funktioner i autofagi [43]. Derfor er RABGAP'er, herunder TBC (TRE2-BUB2-CDC16) domæneholdige RABGAP'er, også involveret i autofagi. RAB33B påvirker dannelsen af autofagosomer ved at rekruttere Atg12-Atg5-Atg16L1-komplekset til fagocytter, og Atg16L1 er bindingsproteinet for RAB33B [44].
En undersøgelse viste, at OATL1 er en GAP, der virker på RAB33B, og dens overekspression kan forsinke autophagosommodning ved at regulere fusionen mellem autophagosomer og lysosomer [45]. RalA/B (RAS ligesom A/B), et medlem af Ras GTPase-familien, er også en nøgleregulator for vesikeltransport [46]. I pattedyrcellemodellen inducerer RalB og dets effektorprotein Exo84 sammen ULK1-Beclin1-VPS34-samling, som er påkrævet for autophagosomdannelse. Under eksperimentelle forhold, der mangler næringsstofbegrænsning, kan et fald i RalGAP aktivere RalB og inducere en stigning i autofagi [47]. I et andet eksperiment med Drosophila som model fandt forskerne ud af, at Ral GTPase regulerer autofagi i forbindelse med PCD [48], som kunne betragtes som ADCD.
Det mekanistiske mål for rapamycin (mTOR) integrerer vækstfaktorer og næringsstofsignaler for at hæmme autofagi. mTORC1, som er et signalkompleks med mTOR som hovedkomponenten, fremmer phosphoryleringen af ULK1 (unc-51-som kinase 1) i nærværelse af tilstrækkelige næringsstoffer [49]. Under regulering af AKT- og AMPK-signalkinaser fungerer tuberøs sklerosekompleks 1/2 (TSC1/2) som GAP for Rheb (Ras-homologen beriget i hjernen) for at hæmme dannelsen af GTP-bundet Rheb og deltager i reguleringen af Rheb-mTORC1-ULK1-signalvejen for at fremme autofagi [49-51]. Tsc1/2-mangel er ansvarlig for udviklingen af tuberøs sklerosekompleks (TSC), en autosomal dominant lidelse, der disponerer patienter for udvikling af tumorer i flere organsystemer [52]. Derfor kan defekt autofagi i TSC føre til akkumulering af autofagiske substrater, herunder unormale proteiner og organeller, i cellen, hvilket fremmer tumorigenese. Undersøgelser har også vist, at deletionen af RalGAP inducerer en stigning i mTORC1-aktivitet, hvilket fører til et fald i autofagi.

I mellemtiden, i bugspytkirtelkræft, undertrykker RalGAP tumorcelleinvasion gennem mTORC1-signalering [53]. Autofagi øger tumorcellernes modstand mod kemoterapi og strålebehandling. Temozolomid (TMZ) til behandling af glioblastom (GBM) er tilbøjelig til at inducere autofagi og kan gøre tumorceller resistente over for lægemidlet. DAB2IP viste sig at regulere ATG9B-ekspression negativt gennem Wnt/-catenin-signalvejen og derved hæmme TMZ-induceret autofagi og øge lægemiddelfølsomheden i GBM-celler [54]. Derudover har DAB2IP også vist sig at være en negativ regulator af autofagi-relateret strålingsmodstand i PCa. Som en opstrøms regulator af DAB2IP nedregulerer miR-32 proteinniveauet af DAB2IP ved at målrette dets 3'-UTR og hæmme dets translation [55]. Efterfølgende aktiveres nedstrøms mTOR-S6K-vejen, men autofagiaktiviteten øges, hvilket kan være resultatet af negativ feedback-hæmning af Akt [56], hvilket i sidste ende forbedrer strålingsmodstanden for PCa-celler [55, 57].
Nogle GAP'er påvirker nervesystemet ved at regulere autofagi. SIPA1L2, et Rap GTPase-aktiverende protein, regulerer processen med frigørelse af neurotransmitter, som er forbundet med TrkB/Rap1-signalering og amfisomer, der er fusionsorganellerne af TrkB-sene endosomer med autofagosomer [58], mens andre, herunder TBC1D5 og TBC1D15, er forbundet med motorneuronsygdom, og disse GAP'er forårsager den lidelsesnedbrydelige proces med autofagi og aggregering af toksiske proteiner [59-63]. SGSM3/RABGAP5 og TBC1D10A inaktiverer begge de tilsvarende GTPaser for at afslutte autofagi og har effekter på immunsystemet, når autofagi eliminerer patogener og beskadiger cellernes organeller [64, 65]. Fraværet af GAP'er kan føre til genetisk heterogene autosomale sygdomme. For eksempel kan deletion af TBC1D20-proteinet øge ulykkesraten for Warburg Microsyndrom 4, som er en autosomal lidelse og har unormale øjen-, hjerne- og genitale funktioner [66]. Autofagi er også en iboende mekanisme til at opretholde stofskiftet og genbruge næringsstoffer under sult eller stress. TBC1D5 binder og sekvestrerer LC3 plus autofagiske rum og øger glukosetransportør GLUT1/Slc2a1-ekspression på plasmamembranen, hvilket letter glukoseoptagelse og glykolytisk flux [67].
Som konklusion nedregulerer de fleste GAP'er den tilsvarende GTPase-aktivitet for direkte at regulere autofagi for at påvirke vores fysiske funktioner, men få tjener som effektorer til indirekte at regulere autofagi for at nå dette mål. Autofagi er tæt forbundet med fysisk homeostase og sundhed. Det er væsentligt, at GAP'er påvirker processen med autofagi. Desværre har ADCD selv mange uudforskede områder, og som følge heraf er der få undersøgelser om ADCD og GAP'er. Vi kan kun udlede den mulige rolle af GAP'er i ADCD fra forbindelsen mellem autofagi og GAP'er. Derfor er yderligere undersøgelser nødvendige for at give os en bedre forståelse af, hvordan GAP'er regulerer ADCD i fysiologiske og patologiske situationer, korrekt forstå patologisk udvikling og finde terapeutiske mål.
Ferroptose
Ferroptosis er en ny oxidativ RCD, hvor konsekvenserne akkumuleres af dødelig jernafhængighed af lipidhydroperoxider [68]. Dens videnskabelige observation initierer eksperimentet med elastin-induceret selektiv celledød i 2003, og udtrykket "ferroptosis" blev opfundet i 2012 [69]. Bagefter genererede forskere en stigning i ferroptoseforskning. Det unikke træk ved dets morfologi er mitokondrielle ændringer, der inkluderer lille størrelse, ændring af membrandensiteter, reduktion eller forsvinden af mitokondriel crista og brud på ydre membraner [70]. Ferroptose er forbundet med en række sygdomme, herunder akut nyreskade, kræft og hjerte-kar-sygdomme. En del af induktionen af ferroptose er RAS-afhængig [71]. I Ras-mutante cancerceller hæmmer blokering af RAS-RAF-MEK-vejen ferroptose induceret af elastin, som er et antitumorlægemiddel, der fremmer celledød [72]. Der er dog relativt lidt kendt om sammenhængen mellem GAP'er og ferroptose.
Et stort antal molekylære markører og veje er blevet beskrevet for autofagi som mulige processer af ferroptose [9, 73]. GTPaser og GAP'er, der spiller en rolle i autofagi, kan også være regulatorer af ferroptose. RAB7A er involveret i den autofagi-inducerede nedbrydning af lipiddråber (LD'er), og den ledsagende lipidperoxidation forværrer ferroptose [74]. Følgelig kunne TBC1D2, som en negativ regulator af RAB7A, regulere ferroptose på en RAB7A-afhængig måde [75]. G3BP1 (Ras-GTPase-aktiverende proteinbindende protein 1) er involveret i justeringen af Ras-signalvejen. Processen med it-induceret celledød er forbundet med det lange ikke-kodende RNA P53RRA, som er reguleret af LSH og p53. Under denne proces interagerer nukleotid 1 og 871 af P53RRA direkte med RNA-genkendelsesmotivets interaktionsdomæne af G3BP1 (aa 177-466), og danner P53RRA-G3BP1-komplekset. I cytoplasmaet fortrænger P53RRA-G3BP1-interaktionen p53 fra et G3BP1-kompleks, hvilket fører til omfordelingen af p53 gennem p53-overførsel fra cytoplasmaet til kernen, hvilket aktiverer p53-signalvejen og påvirker ekspressionen af flere metaboliske gener, såsom TIGAR og SLC7A11, hvilket til sidst forårsager cellecyklusstop, hvilket fører til apoptose og ferroptose [76].
Pyroptose
Pyroptose er en type inflammatorisk RCD, der er en medfødt immunmekanisme til at modstå patogeninvasion og opretholde fysisk homeostase [77]. Caspase-1/4/5/11-aktivering induceres af nogle inflammasomer, som øger spaltningshastigheden af gasdermin D og udskiller modne inflammatoriske cytokiner, såsom interleukin-18 og interleukin-1 [78 ]. Dens funktioner er DNA-fragmentering, cellehævelse og bobler, der i sidste ende sprænger plasmamembranen.
Forbindelsen mellem pyroptose og GAP'er afspejles i celledøden induceret af visse mikroorganismer. YopE er en type Yersinia ydre protein (Yops) og kan fungere som vært GAP for Rho GTPase ved at hydrolysere GTP-bundet Rho GTPase på en ikke-kovalent måde i Yersinia. Under Yersinia-infektion og celledødsinduktion har YopE en anden samarbejdspartner, YopT, en cysteinprotease, der kovalent nedbryder C-terminalen af Rho GTPase, hvilket derfor fører til Rho GTPase-dissociation og inaktivering. Selvom YopE og YopT er væsentligt forskellige fra Rho GTPase-inaktivering, er begge Rhomodificerende toksiner, der påvirker værtscellefysiologien og undgår immunresponser. Denne proces induceres direkte på en måde, der dephosphorylerer de aktive Ser205- og Ser241-steder i pyrin og danner et pyrin-inflammasom, hvilket i sidste ende fører til pyroptose [79].
Entosis celledød
I 2007 beskrev forskere den ikke-apoptotiske celledødsproces entose for at tage højde for det cellespisende fænomen, der observeres mellem tumorceller [80, 81]. Når levende celler forbruges af de samme eller forskellige typer celler, opstår en "celle i en celle" struktur, hvilket resulterer i døden af internaliserede celler (entotiske celler). Døende entotiske celler har ikke de morfologiske og molekylære karakteristika af apoptose, men udviser autofagiafhængighed, med lysosom- og vakuolær membranautofagi-proteinafhængig fusion, der inducerer entose [82, 83].
Celleadhæsion og cytoskeletomlejring er nøgleprocesser i entose og kan ikke defineres i epitelial cadherin og Rho-ROCK-signalering [80]. Rekrutteringen af p190A RhoGAP ved celle-celle-forbindelser hæmmer aktiviteten af Rho-banen, hvilket fører til et fald i myosin let kæde-phosphorylering, hvilket reducerer actomyosin-kontraktion og undertrykker calmodulin-niveauer. På grund af den polariserede fordeling af p190A RhoGAP er kontraktionen af actin ved den distale ende af celleadhæsion signifikant højere end på celleadhæsionsstedet [84]. Derudover aktiveres Rho af RhoGEF i den distale ende af celleadhæsion [85]. Derfor virker RhoGAP og RhoGEF separat for Rho, men synergistisk for induktion af ketose.

Mitotisk katastrofe
Mitotisk katastrofe (MC) er en form for unormal mitotisk celledød, der også er en effektiv anticancermekanisme og terapi [86]. Dets morfologiske karakteristika er unikke nukleare ændringer, der normalt udviser multinukleation og/eller mikronukleation [87]. For at være præcis er MC ikke en type RCD, fordi MC, ligesom autofagi, ikke nødvendigvis forårsager celledød, og derfor anbefaler Nomenklaturudvalget for Celledød 2018 at bruge udtrykket mitotisk død som navnet på denne type død [10 ]. Desuden har undersøgelser vist, at den ultimative skæbne for de fleste MC-celler er iboende apoptose [10, 88], med forskelle og forbindelser mellem de to.
Trætyper af GAP'er er forbundet med afvigende mitose: RasGAP NF1, p190RhoGAP og RanGAP. Mutationer i NF1 kan aktivere RAS-relaterede downstream-signalveje. I dette tilfælde er koordinering af andre signalveje, såsom PKC-relaterede veje, nødvendig for at regulere den cellulære forstyrrelse af RAS-overaktivering og nødvendig for at sikre celleoverlevelse. Under Nf1-mangeltilstande samarbejder undertrykkelsen af endogen proteinkinase C (PKC) højst sandsynligt med Akt (en af downstream-effektorerne af aberrant Ras)-vejen for at aktivere Chk1, forlænge mitotisk standsning og forårsager efterfølgende apoptose via MC [89]. Overekspression af flere kopier i T-celle malignitet 1 (MCT-1) konfronterer præsentationen af PTEN-genet og påvirker negativt stabiliteten og funktionelle aktivitet af dets proteiner, hvilket aktiverer phosphoinositide 3 kinase/AKT-signalering. Derudover nedregulerede MCT-1 p190RhoGAP og opregulerede ekspressionen af p190B, som binder Src, interagerer med MCT-1 og aktiverer Src/p190B-signalering. I sidste ende øger den øgede præsentation af MCT-1 og det hæmmede PTEN synergistisk Src/p190B-vejen, hvilket forårsager depression af RhoA-aktivitet og øger forekomstfrekvensen af MC [90].
I modsætning til beskrivelsen af ovenstående GAP'er, ud over at kinetochore og spindellokalisering af RanGAP1 er påvirket af importin 1, som er en regulator involveret i vektoren af de vigtigste interfasekerner og mitotiske progression, er RanGAP1 sumoylering også relateret til importin 1 og viser en positiv sammenhæng. Mekanismen er mest sandsynlig, at RanBP2 interagerer direkte med N-terminalen af importin 1, sekvestrerer endogent RanBP2, reducerer det og importin 1 og diffunderer begge, hvilket fører til unormal spindeldannelse og svækket kromosomjustering, hvilket i sidste ende forårsager celledød [91] . Sammenfattende kunne den unormale regulering af den tilsvarende GTPase-proteinaktivitet af GAP'er forstyrre den normale signalkaskade og til sidst øge antallet af MC-uheld.
Metoder
Methuosis er en unik form for RCD, og dens særlige karakter er vakuolisering, akkumulering af vesikler (enkeltmembran og fra makropinosomer, der adskiller strukturen af dobbeltmembraner af autophagosomer) og til sidst plasmamembranbrud [92]. Methuosis er tæt forbundet med Ras-signalvejen (kontinuerlig aktivering), som er karakteriseret ved GBM og gastrisk karcinom [93].
GIT1 tjener som GAP til at inaktivere Arf6 ved at hydrolysere GTP for at påvirke metoder. I den proces aktiverer hyperaktive H-Ras Rac1 GEF, hvilket øger mængden af Rac1-GTP. Mikropinocytose forstærket af aktiveringen af Rac1 og clathrin-uafhængig endocytose (CIE) opnår nogle træk ved sene endosomer (Rab7 og LAMP1). I mellemtiden er der en feedbackmekanisme, hvor hyperaktiv Rac1 gør det muligt for Rac1-GTP at interagere direkte med GIT1, hvilket reducerer aktiviteten af Arf6, forringer genanvendelsen af CIE'er og undlader at fusionere med lysosomer. Endelig fører disse konsekvenser til akkumulering af CIE, og sene endosomale vesikler smelter sammen og danner således større væskefyldte cytoplasmatiske vakuoler, som i sidste ende sprænger plasmamembranen og forårsager celledød [94, 95]. Ovenstående resultat modsiger imidlertid Shliom og kollegers finansiering, at Arf6 (Q67 L) aktivitet fremmer vakuoldannelse i celler, der udtrykker H-Ras (G12V) [96]. Den mest passende forklaring på dette fænomen er, at de påvirker de vakuoler, der opstår
GAP'er regulerer tumorimmunitet
RCD og immunitet er tæt forbundet
RCD blev oprindeligt anset for at være en immuntolerogen hændelse, især apoptose [97]. Senere beviser og introduktionen af begrebet immunogen celledød (ICD) har dog gradvist etableret rollen af immunaktivitet i RCD. ICD er ikke en uafhængig dødsmåde, og den refererer til en type RCD, der har tilstedeværelsen af adaptiv immunitet drevet af aktiveringen af cytotoksiske T-lymfocytter (CTL'er) som reaktion på stress-induceret celledød [97, 98]. Udviklingen af ICD er en kompleks proces, hvor eksistensen af antigener, der ikke er dækket af central tolerance i døde celler, og eksponeringen og frigivelsen af skadesassocierede molekylære mønstre (DAMP'er) er nøglekomponenter, omtalt som henholdsvis antigenicitet og adjuvansitet [98 ]. DAMP'er fremmer rekruttering og modning af antigen-præsenterende celler (APC'er), hvilket udløser et CTL-afhængigt immunrespons [99]. Nogle konventionelle kemoterapeutiske midler, onkolytiske vira, målrettede anticancermidler, specifikke strålebehandlingsmodaliteter og andre faktorer kan være inducere af ICD [100, 101].
Baseret på dette fund foreslog forskere i 2013, at kombinationer af ICD-inducere med andre immunmodulatorer kunne føre til effektive antitumoreffekter [99], og efterfølgende undersøgelser har bekræftet, at monoklonale antistoffer rettet mod klassisk hæmmede immunkontrolpunkter, såsom cytotoksiske T-lymfocyt-associerede antigen 4 (CTLA-4), programmeret celledød-1 (PD-1) og dets tilsvarende ligand PD-L1, er gode samarbejdspartnere for ICD [102-104]. For nylig har cancerimmunterapi kombineret med nanoteknologi til at inducere ICD også vist nye perspektiver [105, 106]. Selvfølgelig er andre RCD'er ikke enden af cellen, men kan være begyndelsen på et immunrespons eller endda en ICD [107]. Desuden er disse RCD'er også involveret i antitumorimmunitet [108, 109]. For eksempel medierer T-celler og ferroptose hinanden i tumorer. Immunterapi-aktiverede CD8 plus T-celler øgede lipidperoxidation i tumorceller, hvilket igen bidrog til antitumoreffektiviteten af immunterapi med øget ferroptose [110]. Dette bevis er tilstrækkeligt til at påvise, at RCD er uløseligt forbundet med immunaktivitet og immunterapi.

GAP'er bidrager til immunmikromiljøet
Dannelsen og basalfunktionen af flere immunceller påvirkes af GAP'er (fig. 4A). T-celler er grundpillen i antitumorimmunitet. Umodne dobbeltpositive (DP) thymocytter differentieres delvist til CD4 plus eller CD8 plus enkeltpositive (SP) T-celler efter positiv selektion, hvorimod de andre DP T-celler gennemgår apoptose. Mekanismen, hvorved Ras-MAPK-vejen regulerer denne proces, er blevet grundigt undersøgt [111, 112].
I RASA1-deficient thymus har DP-celler øget modtagelighed for apoptose, men det øgede CD4 SP til DP-forhold tyder på, at RASA1-deletion fremmer positiv selektion og kan være forbundet med Ras-MAPK-signalvejaktivering [113]. I betragtning af den proapoptotiske effekt af DAB2IP nedregulerer CCR 4-NOT-komplekset desuden DAB2IP til at deltage i den positive selektion af thymocytter [114]. Interessant nok viste en anden undersøgelse, at NF1 fremmer en positiv selektion af thymocytter i hun HY TCR Tg mus, men mekanismen er uklar [115]. Et andet eksempel på T-celleregulering er, at ARHGAP19 koordinerer den cytoskeletale remodellering, der kræves til T-lymfocytdeling og kontrollerer kromosomadskillelse ved at regulere RhoA [116]. ARHGAP45 kunne regulere RHO til at orkestrere ændringer i cytoskelettet af naive T-celler, øge deres deformation og migration til lymfeknuder (LN'er) og fremme thymisk udsåning af T-celle-stamceller [117].
Derudover er Rab35 og dets GAP EPI64C (TBC1D10C) påkrævet i dannelsen af immunologiske synapser (IS'er), som er en del af T-celle-APC-interaktionen [118]. Makrofager spiller en nøglerolle nedstrøms for immunresponset ved at opsluge døde celler. Tidligere undersøgelser har karakteriseret Rho GTPase-medlemmerne Rac1 og Cdc42 som molekylære omskiftere, der kontrollerer actin-cytoskeletvæv for at regulere Fc-receptor-medieret fagocytose [119, 120]. Sh3BP1, ArhGAP12 og ArhGAP25 inaktiverede i samarbejde Rac og Cdc42 i tid og rum og afsluttede dermed fagocytose af makrofager til store partikler såsom apoptotiske celler [121]. Makrofager polarisering, motilitet og cellespredningsegenskaber er forbundet med RASA1-medieret regulering af p190RhoGAP translokation [122]. En anden RhoGAP-myosin Myo9b-deletion i makrofager blev vist at resultere i ændret cellemorfologi og nedsat migrationskapacitet [123]. RhoGAP-familiens rolle i neutrofiler er mere omfattende og involverer hovedsageligt neutrofile formændringer, adhæsion, kemotaksi og fagocytose, som gennemgået af Roland Csépányi-Kömi et al. [124].

Med inddragelse af tumormikromiljøet kan tumorceller undslippe overvågningen af immunsystemet og dermed overleve immunangreb under udviklingsprocessen. NF1, der koder for neurofibromin, er et godt eksempel til at illustrere rollen af GAP'er i tumorimmunmikromiljøet (fig. 4B). Neurofibromin er et GTPase-aktiverende protein, der nedregulerer RAS-aktivitet, og mutationer i NF1 kan således aktivere RAS-relaterede downstream-signalveje. Neurofibromatosis type 1 (NF1) er en genetisk lidelse i nervesystemet forårsaget af tab af aktivitet af neurofibrominproteinet GAPs [125]. Immunceller såsom infiltrerende inflammatoriske mastceller er en komponent af NF1, og mutationer af NF1-genet i immunceller er også essentielle for denne sygdom [126]. Forskere designet NF1fox/−; Krox20- Cre-mus med NF1−/− Schwann-celler og NF1 plus /−-mastceller og fandt ud af, at mus med Schwann-celleproliferation såvel som massiv mastcelleinfiltration udviklede plexiforme neurofibromer sammenlignet med kontrolmus. Dette fund viser det faktum, at haploinsufficiensen af NF1-mastceller skaber et NF1 plus /− immunmikromiljø, der favoriserer tumorer [127].
Derudover øger NF1-/- Schwann-celler Nf1-haploinsufficiens mastcellemigration ved stamcellefaktor (SCF) og degranulering gennem c-kit-medieret aktivering af PIK-3-vejen [128-130]. Sammenlignet med normale mennesker er NF1-patienter tilbøjelige til at udvikle tumorer i centralnervesystemet. I lavgradigt gliom (LGG) har forskere opdaget en central neuroimmun akse, som tyder på, at NF1 mutante neuroner producerer midkine for at inducere T-celler til at aktivere mikroglia til at producere CCL5, en faktor, der fremmer væksten af LGG [131]. Lignende resultater blev fundet i GBM.
En nylig undersøgelse viste, at tumormodeller med kodeletion af Nf1 og Pten og overekspression af EGFRVIII kunne undslippe immunclearance og en høj grad af det immunsuppressive mikromiljø, og Nf1-tab var nøglebegivenheden [132]. Interessant nok, selvom den ufuldstændige mutation af NF1-alleler er en drivkraft for tumorer, præsenterer nogle forskere en selvmodsigelse, idet fraværet af NF1 i T-celler kunne øge T-celleaktiviteten for at forbedre tumorens fysiske immunovervågningsmekanisme og hæmme malign migration. I overensstemmelse med dette fund ombygger det kliniske fænomen af NF1-patienter, hvor de fleste tumorer forbundet med NF1 er ikke-maligne, vores anerkendelse af NF1-genmutationer [133].
Derudover har undersøgelser vist, at det Ras-proteinaktivator-lignende 1-protein (Rasal1) negativt regulerer P21Ras-ERK-vejen i T-celler og derved hæmmer aktiveringen af T-celler for at reducere antitumorimmuniteten af T-celler, mens RASAL1-knockdown blev vist. at øge antitumoraktiviteten af T-celler i B16-melanom og EL-4-lymfom [134]. Som GAP af G-proteiner er RGS-familien involveret i reguleringen af immunaktivitet på mange måder og har potentiale for målrettet immunterapi [135]. Nylige undersøgelser har vist, at RGS1 hæmmer transporten af T1-celler og CTL'er til tumorer, hvilket letter dannelsen af 'kolde tumorer' i brystkræft og svækker antitumorimmunitet [136]. I mellemtiden viste museeksperimenter, at overførsel af tumorspecifikke CTL'er med RGS1 knockdown i kombination med PD-L1 kunne være en lovende immunterapeutisk strategi for brystkræft [136].
Konklusioner og perspektiver
Forskningen i GAP'er i sygdomme, især kræft, er steget i de senere år. Nogle GAP'er kan være indflydelsesrige faktorer i cancercelleproliferation, migration, lægemiddelresistens og malign transformation og kan endda være nye terapeutiske mål og prognostiske markører for cancer. Signalvejene forbundet med RCD kunne tunes af GAP'er under denne proces. Det mest typiske eksempel er hæmningen af RAS-relaterede veje af RASGAP'er for at regulere den apoptotiske proces i cancerceller. Undersøgelser af regulering af tumorimmunitet med GAP'er er begrænsede. Her, ved at opsummere den brede rolle af GAP'er i reguleringen af RCD, spekulerer vi i, at det kunne være muligt, at GAP'er er til stede i RCD-relateret immunaktivitet eller mere præcist i ICD-inducerede antitumorimmunresponser. Derudover er GAP'er udtrykt i immunceller essentielle for at opretholde immuncellers fysiologiske funktioner og deltager i immununddragelse og antitumorimmunitet ved at regulere immunceller.
Et af aktiveringskendetegnene for onkogene RAS-proteiner er evnen til at hæmme apoptose af cancerceller for at opnå ubegrænset spredning. Onkogen RAS kan have mutationer, der modstår den hydrolytiske hæmning udløst af RASGAP'er.
Selvom søgningen efter småmolekylære lægemidler, der kunne fungere som ækvivalenter til GAP'er for at fremme RAS-GTP-hydrolyse, længe har været foreslået, er der ikke gjort nogen optimistiske fremskridt. Det er blevet vist, at semaphorin 4D virker på den GAP-aktive receptor Plexin-B1 for at inaktivere R-Ras og derved regulere integrinaktivering og cellemigration [137]. Der findes yderligere eksempler på regulering af specifikke GAP-aktiviteter. For eksempel opregulerer det syntetiske protein frastødende vejledningsmolekyle A (RGMA) receptor neogenin p120GAP-aktivitet, hvilket fører til inhibering af Ras og dets nedstrøms effektor Akt [138]. Hæmning af RASGAPs funktion kan også forekomme i cancer. Imidlertid er de terapeutiske modaliteter for typisk associeret NF1-sygdom stadig meget vanskelige, og de nuværende strategier involverer for det meste hæmning af RAS/MEK-vejen [139]. Sammenfattende, selvom den grundlæggende funktionalitet af GAP'er er godt forstået, er yderligere undersøgelser nødvendige for bedre at forstå, hvordan GAP'er regulerer biologiske processer, for korrekt at forstå patologisk udvikling og for at identificere terapeutiske mål.
Forkortelser
GAP: GTPase-aktiverende protein; RCD: Reguleret celledød; GEF'er: Guanin-nukleotidudvekslingsfaktorer; GDI'er: Guanin-nukleotid-dissociationshæmmere; RGS'er: Regulatorer af G-proteinsignalering; GPCR: G-proteinkoblet receptor; ACD: Utilsigtet celledød; PCD: Programmeret celledød; DISC: Dødsinducerende signalkompleks; TNF: Tumornekrosefaktor; TRAIL: TNF-relateret apoptose-inducerende ligand; RGS3: Regulator af G-proteinsignalering 3; DLC1: Slettet i levercancer 1; DAB2IP: DOC-2/DAB2 interagerende protein; PITX1: Fosforylering af hypofyse homeobox 1; HCC: Hepatocellulært carcinom; ceRNA: Konkurrerende endogent RNA; PCa: Prostatacancer; ECT2: Epitelcelle transformerende sekvens 2; YAP: Ja-associeret protein; TPR: Translokeret promotorregion; BLBC: Basallignende brystkræft; LV: Lymfekar; ADCD: Autofagi-afhængig celledød; mTOR: Mekanistisk mål for rapamycin; TMZ: Temozolomid; GBM: Glioblastom; G3BP1: Ras-GTPaseaktiverende proteinbindende protein 1; Yops: Yersinia Ydre proteiner; MC: Mitotisk katastrofe; MCT-1: Flere kopier i T-celle malignitet 1; ICD: Immunogen celledød; CTL'er: Cytotoksiske T-lymfocytter; DAMP'er: Skade-associerede molekylære mønstre; APC'er: Antigen-præsenterende celler; DP: Dobbelt positiv; NF1: Neurobromatose type 1; SCF: Stamcellefaktor; LGG: Lavgradigt gliom; Rasal1: Ras-proteinaktivator-lignende 1-protein.
Anerkendelser
Vi takker Prof. Yongguang Tao og Dr. Li Xie og Wenbing Liu for verifikationen af figurerne og manuskriptet.
Forfatteres bidrag
YJ og LC bidrog til udformningen og designet af anmeldelsen. HH og SW skrev manuskriptet. JH og HH udarbejdede figurer og tabel. SJ, LL og YL samlede referencerne og deltog i diskussionen. Alle forfattere læste og godkendte det endelige manuskript
Finansiering
Dette arbejde blev støttet af National Natural Science Foundation of China (81802785 [YJ], 82100490 [LC]), Hunan Provincial Natural Science Foundation of China (2020JJ5382 [YJ], 2020JJ5381 [LC]), Scientific Research Project of Hunan Provincial Health Kommissionen (20200763 [WL]) og grundlæggende forskningsprojekt fra Changsha Science and Technology Bureau (kq2004127 [LX]).

Tilgængelighed af data og materialer
Ikke anvendelig.
Erklæringer
Etisk godkendelse og samtykke til deltagelse
Ikke anvendelig.
Samtykke til offentliggørelse
Ikke anvendelig.
Konkurrerende interesser
Forfatterne erklærer, at de ikke har nogen konkurrerende interesser.
Forfatterdetaljer
1 Nøglelaboratoriet for modeldyre- og stamcellebiologi i Hunan-provinsen, Hunan Normal University, Changsha 410013, Hunan, Folkerepublikken Kina. 2 School of Medicine, Hunan Normal University, Changsha 410013, Hunan, Folkerepublikken Kina. 3 Afdeling for hoved- og halskirurgi, Det tilknyttede kræfthospital i Xiangya School of Medicine, Central South University, Changsha 410013, Hunan, Folkerepublikken Kina. 4 Key Laboratory of Carcinogenesis and Cancer Invasion, Ministeriet for Undervisning, Department of Pathology, Xiangya Hospital, School of Basic Medicine, Central South University, Changsha 410078, Hunan, Folkerepublikken Kina.
Referencer
1. Wennerberg K, Rossman KL, Der CJ. Ras-superfamilien på et øjeblik. J Cell Sci. 2005;118(Pt 5):843–6.
2. Takai Y, Sasaki T, Matozaki T. Små GTP-bindende proteiner. Physiol Rev. 2001;81(1):153–208.
3. Bos JL, Rehmann H, Wittinghofer A. GEF'er og GAP'er: kritiske elementer i kontrollen af små G-proteiner. Celle. 2007;129(5):865–77.4. Cherfls J, Zeghouf M. Regulering af små GTPaser af GEF'er, GAP'er og GDI'er. Physiol Rev. 2013;93(1):269–309.
5. Ligeti E, Welti S, Schefzek K. Inhibering og terminering af fysiologiske responser af GTPase-aktiverende proteiner. Physiol Rev. 2012;92(1):237–72.
6. Ross EM, Wilkie TM. GTPase-aktiverende proteiner til heterotrimere G-proteiner: regulatorer af G-proteinsignalering (RGS) og RGS-lignende proteiner. Annu Rev Biochem. 2000;69:795-827.
7. Schefzek K, Ahmadian MR, Kabsch W, Wiesmuller L, Lautwein A, Schmitz F, Wittinghofer A. Ras-RasGAP-komplekset: strukturelt grundlag for GTPase-aktivering og dets tab i onkogene Ras-mutanter. Videnskab. 1997;277(5324):333-8.
8. Schefzek K, Shivalingaiah G. Ras-specifikke GTPase-aktiverende proteiner strukturer, mekanismer og interaktioner. Cold Spring Harb Perspect Med. 2019;9(3):a031500.
9. Tang D, Kang R, Berghe TV, Vandenabeele P, Kroemer G. Det molekylære maskineri af reguleret celledød. Cell Res. 2019;29(5):347–64.
10. Galluzzi L, Vitale I, Aaronson SA, Abrams JM, Adam D, Agostinis P, Alnemri ES, Altucci L, Amelio I, Andrews DW, Annicchiarico-Petruzzelli M, Antonov AV, Arama E, Baehrecke EH, Barlev NA, Bazan NG, Bernassola F, Bertrand MJM, Bianchi K, Blagosklonny MV, Blomgren K, Borner C, Boya P, Brenner C, Campanella M, Candi E, Carmona-Gutierrez D, Cecconi F, Chan FK, Chandel NS, et al. Molecular mechanisms of cell death: recommendations of the Nomenclature Committee on Cell Death 2018. Cell Death Differ. 2018;25(3):486-541.
11. Maiuri MC, Zalckvar E, Kimchi A, Kroemer G. Selvspisning og selvmord: krydstale mellem autofagi og apoptose. Nat Rev Mol Cell Biol. 2007;8(9):741-52.
12. Kerr JF. Krympningsnekrose: en særskilt form for cellulær død. J Pathol. 1971;105(1):13-20.
13. Carneiro BA, El-Deiry WS. Målretning mod apoptose i cancerterapi. Nat Rev Clin Oncol. 2020;17:395-417.
14. Czabotar PE, Lessene G, Strasser A, Adams JM. Kontrol af apoptose af BCL-2-proteinfamilien: implikationer for fysiologi og terapi. Nat Rev Mol Cell Biol. 2014;15(1):49–63.
15. Seyrek K, Ivanisenko NV, Richter M, Hillert LK, Konig C, Lavrik IN. Kontrol af celledød gennem post-translationelle modifikationer af DED-proteiner. Trends Cell Biol. 2020;30(5):354–69.
16. Tai WT, Chen YL, Chu PY, Chen LJ, Hung MH, Shiau CW, Huang JW, Tsai MH, Chen KF. Proteintyrosinphosphatase 1B dephosphorylerer PITX1 og regulerer p120RasGAP i hepatocellulært karcinom. Hepatologi. 2016;63(5):1528–43.
17. Vanli G, Sempoux C, Widmann C. Caspase-3/p120 RasGAP stress-sensing-modulet reducerer forekomsten af leverkræft, men påvirker ikke den samlede overlevelse hos gamma-bestrålede og carcinogenbehandlede mus. Mol Carcinog. 2017;56(6):1680–4.
18. Yang JY, Michod D, Walicki J, Murphy BM, Kasibhatla S, Martin SJ, Widmann C. Delvis spaltning af RasGAP med caspaser er påkrævet for celleoverlevelse under milde stressforhold. Mol Cell Biol. 2004;24(23):10425-36.
19. Lu S, Zhou J, Sun Y, Li N, Miao M, Jiao B, Chen H. Det ikke-kodende RNA HOXD-AS1 er en kritisk regulator af metastase- og apoptosefænotypen i humant hepatocellulært karcinom. Mol Cancer. 2017;16(1):125.
20. Guo X, Xiang C, Zhang Z, Zhang F, Xi T, Zheng L. Displacement of Bax by BMF medierer STARD13 3'UTR-induceret brystcancercellers apoptose på en miRNA-afhængig måde. Mol Pharm. 2018;15(1):63–71.
21. Sánchez-Martín D, Otsuka A, Kabashima K, Ha T, Wang D, Qian X, Lowy DR, Tosato G. Effekter af DLC1-mangel på væksthæmning af endotelceller og progression af angiosarkom. J Natl Cancer Inst. 2018;110(4):390–9.
22. Bellazzo A, Di Minin G, Collavin L. Blok en, slip hundrede løs. Mekanismer for DAB2IP-inaktivering i cancer. Celledød er forskellig. 2017;24(1):15–25.
23. Zhou J, Ning Z, Wang B, Yun EJ, Zhang T, Pong RC, Fazli L, Gleave M, Zeng J, Fan J, Wang X, Li L, Hsieh JT, He D, Wu K. DAB2IP-tab giver anledning til resistensen af prostatacancer mod androgen-deprivationsterapi gennem aktivering af STAT3 og hæmning af apoptose. Celledød Dis. 2015;6:e1955.
24. Yang XM, Cao XY, He P, Li J, Feng MX, Zhang YL, Zhang XL, Wang YH, Yang Q, Zhu L, Nie HZ, Jiang SH, Tian GA, Zhang XX, Liu Q, Ji J, Zhu X, Xia Q, Zhang ZG. Overekspression af Rac GTPase-aktiverende protein 1 bidrager til proliferationen af kræftceller ved at reducere flodhestsignalering for at fremme cytokinese. Gastroenterologi. 2018;155(4):1233–49.
25. Tatsumoto T, Xie X, Blumenthal R, Okamoto I, Miki T. Human ECT2 er en udvekslingsfaktor for Rho GTPaser, phosphoryleret i G2/M-faser og involveret i cytokinese. J Cell Biol. 1999;147(5):921-8.
26. Chen J, Xia H, Zhang X, Karthik S, Pratap SV, Ooi LL, Hong W, Hui KM. ECT2 regulerer Rho/ERK-signalaksen for at fremme tidligt tilbagefald i humant hepatocellulært karcinom. J Hepatol. 2015;62(6):1287–95.
27. Lawson CD, Fan C, Mitin N, Baker NM, George SD, Graham DM, Perou CM, Burridge K, Der CJ, Rossman KL. Rho GTPase-transkriptomanalyse afslører onkogene roller for rho GTPase-aktiverende proteiner i basallignende brystkræft. Cancer Res. 2016;76(13):3826–37.
28. Lapinski PE, Lubeck BA, Chen D, Doosti A, Zawieja SD, Davis MJ, King PD. RASA1 regulerer funktionen af lymfekarventiler hos mus. J Clin Invest. 2017;127(7):2569–85.
29. Wang Z, Huang H, He W, Kong B, Hu H, Fan Y, Liao J, Wang L, Mei Y, Liu W, Xiong X, Peng J, Xiao Y, Huang D, Quan D, Li Q, Xiong L, Zhong P, Wang G. Regulator af G-proteinsignalering 5 beskytter kardiomyocytter mod apoptose under in vitro hjerteiskæmi-reperfusion hos mus ved at hæmme både JNK1/2 og P38 signalveje. Biochem Biophys Res Commun. 2016;473(2):551–7.
30. Wang H, Fan L, Wang H, Ma X, Du Z. Amyloid beta regulerer udtrykket og funktionen af AIP1. J Mol Neurosci. 2015;55(1):227–32.
31. Sirohi K, Swarup G. Defekter i autofagi forårsaget af glaukom-associerede mutationer i optineurin. Exp Eye Res. 2016;144:54–63.
32. Shen HM, Codogno P. Autofagisk celledød: Loch Ness-monster eller truede arter? Autofagi. 2011;7(5):457–65.
33. Kriel J, Loos B. Det gode, det dårlige og det autofagosome: udforskning af ubesvarede spørgsmål om autofagiafhængig celledød. Celledød er forskellig. 2019;26(4):640–52. 34. Lindqvist LM, Simon AK, Baehrecke EH. Aktuelle spørgsmål og mulige kontroverser i autofagi. Celledød Discover. 2015;1:1-7.
35. Amaravadi R, Kimmelman AC, White E. Nylig indsigt i funktionen af autofagi i cancer. Genes Dev. 2016;30(17):1913–30.
36. Kimmelman AC, White E. Autophagy and tumor metabolism. Celle Metab. 2017;25(5):1037–43.
37. Kanzawa T, Kondo Y, Ito H, Kondo S, Germano I. Induktion af autofagisk celledød i maligne gliomceller med arsentrioxid. Cancer Res. 2003;63(9):2103–8.
38. Dasari SK, Bialik S, Levin-Zaidman S, Levin-Salomon V, Merrill AH Jr, Futerman AH, Kimchi A. Signalom-wide RNAi-skærm identificerer GBA1 som en positiv mediator af autofagisk celledød. Celledød er forskellig. 2017;24(7):1288-302.
39. Zein L, Fulda S, Kogel D, van Wijk SJL. Organel-specifikke mekanismer for lægemiddel-induceret autofagi-afhængig celledød. Matrix Biol. 2021;100–101:54–64.
40. Elgendy M, Sheridan C, Brumatti G, Martin SJ. Onkogen Ras-induceret ekspression af Noxa og Beclin-1 fremmer autofagisk celledød og begrænser klonogen overlevelse. Mol Cell. 2011;42(1):23–35.
41. Stenmark H. Rab GTPaser som koordinatorer af vesikeltrafik. Nat Rev Mol Cell Biol. 2009;10(8):513–25.
42. Hyttinen JM, Niittykoski M, Salminen A, Kaarniranta K. Modning af autofagosomer og endosomer: en nøglerolle for Rab7. Biochim Biophys Acta. 2013;1833(3):503–10.
43. Szatmari Z, Sass M. De autofagiske roller af Rab små GTPaser og deres opstrøms regulatorer: en gennemgang. Autofagi. 2014;10(7):1154–66.
44. Pantoom S, Konstantinidis G, Voss S, Han H, Hofnagel O, Li Z, Wu YW. RAB33B rekrutterer ATG16L1-komplekset til phagophoren via et ikke-kanonisk RAB-bindende protein. Autofagi. 2020. https://doi.org/10.1080/ 15548627.2020.1822629.
45. Itoh T, Kanno E, Uemura T, Waguri S, Fukuda M. OATL1, en ny autophagosom-resident Rab33B-GAP, regulerer autophagosomal modning. J Cell Biol. 2011;192(5):839–53.
46. Moskalenko S, Henry DO, Rosse C, Mirey G, Camonis JH, White MA. Exocysten er et Ral-effekterkompleks. Nat Cell Biol. 2002;4(1):66-72.
For more information:1950477648nn@gmail.com






