Del 2: Akut nyreskade hos indlagte børn med seglcelleanæmi
Jun 21, 2022
For mere info. kontakttina.xiang@wecistanche.com
Resultater
Karakteristika for undersøgelsespopulationen
I alt 185 børn med SCA og VOC blev indskrevet i undersøgelsen (fig. 1). Medianalderen var 8,9 år (IQR, 5,9-11,8), og 41,6 procent af deltagerne var kvinder (tabel 1). Forekomsten af underernæring var høj med 30,8 procent af børn, der var forkrøblede (højde-for-alder z-score<-2), 25.9%="" underweight="" (weight-for-age="" z=""><-2),and 29.7%="" wasted="" (weight-for-height="" z="" score="" or="" bmi-for-age="" z=""><-2).of the="" 185="" children="" enrolled,="" 24(13.0%)children="" had="" a="" history="" of="" stroke,="" and="" 78(42.2%)had="" been="" hospitalized="" in="" the="" previous="" six="" months="" (table="" 1).="" the="" majority="" (70.3%)of="" children="" had="" severe="" anemia="" with="" a=""><8 g/dl="" and="" 38="" (20.5%)children="" had="" evi-dence="" of="" an="" acute="" infection="" defined="" as="" sepsis="" (n="19," 10.3%),malaria="" (n="17," 9.6%),="" or="" urinary="" tract="" infection="" (n="4,2.2%).Six(3.2%)of" the="" participants="" died="" during="" hospitalization="" and="" all="" deaths="" occurred="" in="" female="" participants="" (mortality,="">



Den gennemsnitlige varighed af smerte før indlæggelse var 3 dage. De rapporterede steder med smerte omfattede underekstremiteterne (64,9 procent), mave (41,6 procent), øvre lemmer (30,3 procent), ryg (29,7 procent), bryst (34,6 procent) og andre (3,8 procent). Analgesi til børn inkluderede paracetamol (93,0 procent), morfin (86,0 procent), ibuprofen (83,8 procent), diclophenac (10,3 procent), kodein (2,2 procent) og tramadol (1,1 procent).

Klik her for at lære om fordelene ved cistanche tubulosa-ekstrakt
Forekomst af AKI hos børn med SCA
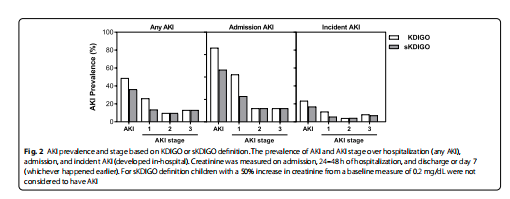
Samlet set havde 90/185 (48,7 procent ) børn AKI ved brug af KDIGO-definitionen med størstedelen afAKI cases occurring on admission 61/90(67.8%)while 34/90(37.8%)children had an incident or worsening AKI over hospitalization (Fig.2).In children with AKI,23/90(25.6%) of cases occurred in children with a baseline creatinine of 0.2 mg/dL that increased to 0.3 mg/dL over hospitalization. Using the sKDIGO definition, 67/185 (36.2%)children had AKI with 26 cases diagnosed based on a 0.3 mg/dL increase in creatinine within 48 h and 41 cases based on a fold increase in creatinine over 7 days;43/67(64.2%) had AKI on admission and 28/67(41.8%)developed incident or worsening AKI during hospitalization (Fig. 2). There were no relationships between medication use and AKI (p>0.05 for alle).
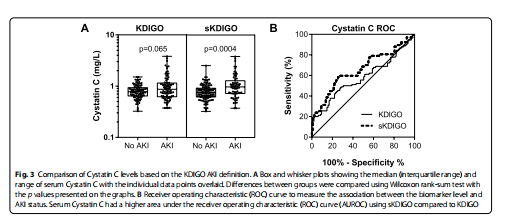
Sammenligning af laboratoriefund og kliniske resultater baseret på KDIGO eller sKDIGO definition af AKI
Vi evaluerede forholdet mellem både AKI-definitioner og klinisk kemi og urinanalyseresultater (tabel 2). Samlet set var forskelle i laboratorieparametre større hos børn, der havde AKI defineret ved hjælp af sKDIGO-definitionen sammenlignet med KDIGO (tabel 2). Vi evaluerede yderligere KDIGO- og sKDIGO-definitionen ved hjælp af Cystatin C, en alternativ markør for GFR (fig. 3). Cystatin C var kun forhøjet hos børn, der opfylder sKDIGO-definitionen af AKI (s<>
Til sidst sammenlignede vi resultater hos børn baseret på AKI-status. AKI var forbundet med øget dødelighed ved brug af sKDIGO (dødelighed, 0.9 procent ingen AKI vs. 7.5 procent AKI, p=0.024), men ikke den oprindelige KDIGO-definition (dødelighed, ingen AKI, 1,1 procent vs.5,6 procent AKI,p=0.110). AKI ved indlæggelse var ikke forbundet med øget dødelighed. Tværtimod havde børn, der udviklede hændelig AKI på hospitalet eller dem med forværret AKI, øget dødelighed (s.<0.05 for="" both).="" as="" the="" skdigo="" definition="" was="" a="" better="" predictor="" of="" mortality,="" subsequent="" analyses="" evaluating="" risk="" factors="" for="" aki="" and="" aki="" progression="" are="" conducted="" using="">
Risikofaktorer for AKI hos børn med SCA og VOC
For at forbedre genkendelsen af AKI hos børn med SCA, som kræver hospitalsindlæggelse, evaluerede vi forskelle i de demografiske karakteristika, tegn og symptomer ved indlæggelse og laboratoriefund hos børn med AKI (tabel 3). Da 43/67 (64,2 procent) børn havde AKI ved indlæggelse på hospitalet, er vi ikke i stand til at tilskrive kausalitet til disse risikofaktorer. Forståelse af risikofaktorer i denne højrisikopopulation kan imidlertid gøre det muligt for klinikere at identificere funktioner, der hæver deres mistankeindeks, hvilket minimerer eksponeringen for potentielle nefrotoksiske midler og prioriterer overvågning hos børn med den højeste risiko for AKI. Ved brug af logistisk regression inkluderede AKI-risikofaktorer alder (aOR, 1,10,95 procent CI1,01, 1,20), hypovolæmi (aOR, 2,98,95 procent CI 1,08, 8,24), øm hepatomegali (aOR, 2,46,95 procent CI 1,75,5,5,5. ), og en akut infektion (aOR, 2,63,95 procent CI1,19, 5,81) (p<>
Risikofaktorer for AKI ved indlæggelse og forværring eller hændelse af AKI under indlæggelse
For at bestemme risikofaktorer hos børn med samfundserhvervet AKI versus hospitalserhvervet eller forværret AKI, stratificerede vi analyser baseret på tidspunktet for diagnose (tabel 4). Børn med samfundserhvervet AKI var ældre og var mere tilbøjelige til at have te-farvet urin og hepatomegali eller øm hepatomegali. Derudover var AKI ved indlæggelse forbundet med hypovolæmi og en akut infektion, og laboratoriefund var i overensstemmelse med en akut inflammatorisk hændelse. I modsætning hertil var deltagere med en hændelse eller forværring af AKI i forhold til hospitalsindlæggelse ens i alder, med sammenlignelige infektionsfrekvenser og lignende laboratoriefund. Der var ingen forskelle i brug af nefrotoksisk medicin hos børn med en hændelse eller forværring af AKI (tabel 4). Deltagere, der udviklede hændelser eller forværrede AKI, var mere tilbøjelige til at være kvinder.

Diskussion
Mens AKI er en anerkendt klinisk komplikation af VOC hos børn med SCA [8], er der en mangel på prospektive undersøgelser, der evaluerer forekomsten af AKI hos børn med SCA fra LMIC. I denne undersøgelse brugte vi KDIGO konsensus retningslinjerne til at definere AKI hos børn med SCA præsenteret med VOC, ved brug af serielle kreatininmålinger over hospitalsindlæggelse. I betragtning af procentdelen af børn, der havde lave kreatininværdier som følge af hyperfiltrering og underernæring, overvejede vi også sKDIGO-definitionen. Samlet set var sKDIGO forbundet med højere dødelighed sammenlignet med den oprindelige KDIGO-definition. Risikofaktorer for AKI ved indlæggelse omfattede ældre alder, en akut infektion, øm hepatomegali, hypovolæmi og te-farvet urin.
SCA er forbundet med en række nyreabnormaliteter, herunder hyperfiltrering, papillær nekrose,glomerulosklerose, ogkronisk nyresygdom, som tilsammen kan disponere mennesker, der lever med SCA for AKI [8]. Ved brug af sKDIGO havde 36,2 procent af deltagerne AKI med 13,5 procent trin 1,9,7 procent trin 2 og 13.0 procent trin 3. Forekomsten af AKI i denne undersøgelse er højere end tidligere undersøgelser, der rapporterede en AKI-prævalens på mellem 2,5 procent til 17 procent hos børn indlagt med VOC [4-7]. Disse undersøgelser blev dog stort set udført i højindkomstlande. Børn med SCA i LMIC'er kan have yderligere risikofaktorer, der påvirker et barns risiko for at udvikle AKI under indlæggelse [9], herunder endemiske infektioner som malaria, der bidrager til betydelig AKI hos ugandiske børn [22-24]. Størstedelen af AKI i denne undersøgelse var fællesskabserhvervet AKI og i overensstemmelse med globale tendenser til øget fællesskabserhvervet AKI i LMIC[25].
AKI ved indlæggelse var forbundet med manglende evne til at drikke eller amme, opkastning og diarré, som er risikofaktorer for hypovolæmi og prærenal AKI. Infektioner kan øge AKI-risikoen ved at forværre dehydrering og hypovolæmi gennem øgede ufølsomme tab sekundært til feber. Infektioner - især malaria og sepsis - er almindelige hos børn med SCA i LMIC'er og bidrager til signifikant morbiditet og dødelighed hos disse børn [9]. Malaria og sepsis er veletablerede risikofaktorer for AKI [23,26], der kan forværre mikrovaskulær dysfunktion i VOC'er, da endotelaktivering kan føre til mikrovaskulær dysfunktion, inflammation og frigivelse af endogene nefrotoksiner som cellefri hæmoglobin og fri hæm, der øger oxidativ stress og bidrager til tubulær skade [27-31]. Infektioner er en risikofaktor for VOC hos børn med SCA, så forbedret infektionsforebyggelse kan reducere byrden af SCA-relaterede komplikationer, herunder AKI. Ydermere, da børn med SCA modtager rutinemæssig klinisk opfølgning gennem seglcelleklinikken, undervisning i forebyggelse af dehydrering og rådgivning om, hvordan man på passende vis kan håndtere smerter og feber derhjemme, samtidig med at eksponeringen for nefrotoksiske midler som non-steroide minimeres.anti-inflammatorisklægemidler kan reducere byrden af samfundserhvervet AKI.
I denne undersøgelse forekom alle undersøgelsesdødsfald hos kvinder med en historie med at have passeret tefarvet urin (et træk ved hæmoglobinuri), og at være kvinde var forbundet med udviklingen af hændelse eller forværring af AKI. Yderligere undersøgelser er nødvendige for at forstå sociale og biologiske determinanter for sundhed i denne befolkning. Der var en tendens til øget hæmoglobinuri hos kvinder (49,4 procent) sammenlignet med mænd (35,9 procent). Ud over at være en risikofaktor for dødelighed var hæmoglobinuri også en risikofaktor for AKI ved indlæggelse. Hæmoglobinuri er en almindelig komplikation hos børn med SCA forbundet med igangværende hæmolyse og er forbundet med progression til kronisk nyresygdom (CKD)[32]. Selvom ætiologien af hæmoglobinuri hos børn med AKI kan tilskrives igangværende hæmolyse, er der rapporter om en stigende forekomst af hæmoglobinuri (sortvandsfeber) i Uganda [33, 34]. Sortvandsfeber forekommer ofte hos børn med anæmi og en historie med malariainfektion og er en kendt risikofaktor for AKI ved svær malaria [35-37] og er forbundet med øget morbiditet og dødelighed efter udskrivelsen.

AKI er defineret ved reduceret urinproduktion eller en stigning i serumkreatinin. I forbindelse med denne undersøgelse blev AKI defineret baseret på serumkreatinin alene, da data om urinproduktion ikke var tilgængelige. Det er udfordrende at definere AKI hos børn med SCA, da glomerulær hyperfiltration og øget tubulær sekretion af kreatinin påvirker serumkreatininniveauer [8]. Desuden påvirkes kreatinin af ikke-renale faktorer som muskelsvind [38-40]. Underernæring var almindelig i undersøgelsen med 29,7 procent af befolkningen spildt. Da den præ-morbide baseline kreatinin ikke var kendt i undersøgelsespopulationen, anvendte vi deltagernes individuelle baner. Øget adgang til kreatinintestning og mere rutinemæssig kreatinintestning hos børn med SCA ville muliggøre en mere præcis klassificering af AKI hos børn under akutte infektioner eller VOC. I denne undersøgelse blev Cystatin C forhøjet hos børn med AKI, hvilket fremhæver, at AKI er forbundet med både funktionelle ændringer i filtration såvel som tubulær skade [41]. Yderligere forskning er nødvendig for at evaluere alternative biomarkører for AKI hos børn med SCA.
This study evaluated AKI during single hospital admission for a VOC. However, children often have multiple occurrences of VOC annually [42,43]. Currently, the Uganda clinical guidelines recommend the initiation of hydroxyurea in children with frequent VOC (>5 episoder om året). I NOHARM-forsøget blev der registreret 308 VOC hos 88 deltagere over et år [17]. Med en prævalensrate på AKI på 36,2 procent hos børn, der blev evalueret for en enkelt episode af VOC, er børn med SCA i risiko for gentagne AKI-episoder. I en stor hospitalsbaseret undersøgelse af sorte amerikanere var flere smertekriser årligt forbundet med et hurtigere fald i glomerulære filtrationshastigheder (GFR) sammenlignet med patienter med SCA uden hyppige smertekriser. AKI er en etableret risikofaktor for udvikling af CKD [45-48]. Yderligere har personer, der lever med CKD, øget risiko for AKI, hvilket yderligere kan accelerere progressionen af CKD [49]. Denne undersøgelse fremhæver behovet for yderligere undersøgelser for at evaluere forekomsten af AKI over flere år hos børn med SCA for at forstå, hvordan AKI påvirker udviklingen af CKD i LMIC, hvor størstedelen af børn med SCA bor. Denne information vil være vigtig for at guide udviklingen af retningslinjer for klinisk opfølgning af børn med risiko for CKD efter AKI.
Albuminuria is a risk factor for CKD [50-52] and 20% of study participants had an albumin-to-creatinine ratio>30 mg/mmol tyder på glomerulær skade [49]. SCA er forbundet med en tidlig alder af CKD-debut og et hurtigere fald i GFR [44,53]. I nærværende undersøgelse har 54,6 procent af børnene<5 years="" of="" age="" had="" albuminuria="" with="" 45.5%="" microalbuminuria="" and="" 9.1%="" macroalbuminuria.="" this="" is="" higher="" than="" in="" an="" ongoing="" study="" following="" 2582="" participants="">3 år med SCA i fire vestafrikanske lande, hvor prævalensen af mikro- og makroalbuminuri var henholdsvis 29 procent og 5 procent (medianalder på 14 år)[54]. Yderligere undersøgelser er nødvendige for at vurdere forekomsten af albuminuri hos børn med SCA i steady-state for at bestemme den passende alder til at starte screening for albuminuri. Der er behov for tidlig identifikation af CKD, passende klinisk behandling og tidligere henvisning til specialiserede nyretjenester, der kan have en målbar forbedring af børns sundhed og livskvalitet.
En af undersøgelsens begrænsninger var mangel på steady-state SCr-måling til at estimere baseline serumkreatinin, hvilket afspejler begrænsninger i rutinemæssige SCr-målinger i omgivelserne. Vi vurderede SCr på forudspecificerede tidspunkter for at falde sammen med KDIGO-definitionen af AKI og havde ikke daglige SCr-målinger eller målinger ud over 7 dage, hvilket kan have resulteret i ubesvarede AKI-episoder over hospitalsindlæggelse. Ydermere fandt en nylig prospektiv multinational undersøgelse (AWARE), der vurderede AKI hos kritisk syge børn på 32 pædiatriske intensivafdelinger på tværs af fem kontinenter, at AKI defineret ved hjælp af SCr alene, undlod at identificere AKI hos 67 procent af børn med lav urinproduktion [55] . I denne undersøgelse blev AKI defineret på basis af serumkreatinin alene, og AKI kan derfor være undervurderet, da vi ikke vurderede urinproduktion. Der er behov for yderligere undersøgelser med bredere definitioner af AKI, såsom yderligere brug af urinproduktion til at definere AKI samt længere opfølgningsperioder for at evaluere hændelse af AKI i løbet af hospitalsindlæggelse, vedvarende nyreskade og genopretning af nyrerne. Anerkendelse og validering af AKI-risikofaktorer kan lette identifikationen af børn, der sandsynligvis vil drage fordel af kreatinintestning og målrettede indgreb for at fremme nyrernes genopretning.
Denne undersøgelse har flere styrker, herunder dets prospektive design og den serielle evaluering af kreatinin over hospitalsindlæggelse. Ved at bruge en deltagers individuelle bane for SCr over hospitalsindlæggelse til at definere AKI, undgår vi at fejlklassificere børn med allerede eksisterende kronisk nyresygdom som havende AKI baseret på befolkningsestimater af baseline SCr. Der er få prospektive undersøgelser af AKI hos børn med SCA i LMIC, og denne undersøgelse supplerer den eksisterende litteratur om komplikationer af SCA hos børn. Derudover inkluderede denne undersøgelse en række kliniske laboratorieevalueringer og vurderede biomarkører af AKI, som gjorde det muligt for os at evaluere nytten af forskellige definitioner til at definere AKI. Vores undersøgelse fremhæver behovet for mere målrettede programmer rettet mod forebyggelse og håndtering af både samfundserhvervet og hospitalserhvervet AKI i LMIC'er.

Konklusion
Vores undersøgelse viser, at AKI er en hyppig komplikation af hospitalsindlagte børn med SCA og fremhæver behovet for et øget mistankeindeks hos børn indlagt med en VOC uanset smertens sværhedsgrad. Ændrede KDIGO-retningslinjer (sKDIGO) udelukkede en stigning fra {{0}}.2 til 0.3 som en 1.5--fold stigning i SCr korrelerede bedre med biomarkører afakut nyreskadeog dødelighed end standard KDIGO AKI-retningslinjer, der fremhæver vigtigheden af at tage højde for den hyperfiltrering, der forekommer hos børn med SCA, når AKI defineres. Undersøgelsen bygger på eksisterende litteratur om komplikationer af SCA i LMIC'er og viser, at en betydelig del af AKI'en er fællesskabserhvervet. Der er således behov for interventioner rettet mod forebyggelse og behandling af AKI hos børn med SCA, især under VOC, som ofte er tilbagevendende. Enkle trin, herunder hurtig rehydrering hos børn, der ikke er i stand til at tolerere orale væsker eller med væsketab som følge af diarré eller opkastning, kan reducere AKI-progression, og i denne højrisikopopulation bør nefrotoksiske lægemidler til smertebehandling anvendes med omtanke.
