Mineralokortikoid-receptoraktivering og -antagonisme ved hjerte-kar-sygdomme: cellulære og molekylære mekanismer
Jul 07, 2022
Aldosteron kontrollerer saltvandshomeostase ved at virke på mineralocorticoid-receptoren (MR), en ligand-aktiveret transkriptionsfaktor, i nyreepitelceller. Imidlertid er det nu tydeligt, at MR udtrykkes i flere celletyper og væv, der fungerer som en nøglefaktor for hjerte-kar-sygdomme. MR-antagonister har vist sig at være yderst effektive hos patienter med hjertesvigt og reduceret ejektionsfraktion, og de er en hjørnesten i moderne terapi. I det sidste årti afslørede en række eksperimentelle undersøgelser, der brugte modeller med celletypespecifik MRS, de cellulære og molekylære mekanismer, der ligger til grund for dens skadelige effekt på venstre ventrikel-ombygning. Baseret på disse fund er potentialet for MR-antagonister blevet evalueret i andre kardiovaskulære sygdomme, herunder koronararteriesygdom, arteriel hypertension, hjertesvigt med bevaret ejektionsfraktion, pulmonal hypertension, atrieflimren og hjerteklapsygdom. Nærværende gennemgang opsummerer den nuværende viden om MR-aktivering og antagonisme ved hjerte-kar-sygdomme.

Klik for at maca ginseng cistanche til nyre
Aldosteron, et steroidhormon, der produceres af zona glomerulosa-celler i binyrebarken, er et centralt effektorhormon i renin-angiotensin-aldosteron-systemet.1,2 Den fysiologiske rolle af aldosteron er at kontrollere salt-vand-homeostase ved at virke på mineralocorticoid-receptoren (MR), en ligand-aktiveret transkriptionsfaktor, i nyreepitelceller. Aldosteron via MR fører til opregulering og aktivering af den amiloridfølsomme epiteliale Naþ-kanal, hvorved Naþ-reabsorption og Kþ-sekretion øges.2 Den første MR-antagonist (MRA), spironolacton, blev udviklet som et antihypertensivt lægemiddel, med det formål at forhindre Naþ. fastholdelse og formindskelse af blodvolumen.3,4 Men på grund af dets aktivitet på progesteronreceptoren og andre nukleare receptorer kan spironolacton forårsage relevante bivirkninger, såsom gynækomasti.3 Denne effekt kan forbedres af andengenerationsforbindelsen eplerenon og, for nylig en ny klasse af meget selektive, potente ikke-steroide MRA'er. såsom fifinerenon og esaxerenon.3,4
Johann Bauersachs1 og Achim Lother2,3
1 Afdeling for kardiologi og angiologi, Hannover Medical School, Hannover, Tyskland;
2 Institut for Kardiologi og Angiologi I, University Heart Center, Medical Center – Det medicinske fakultet, University of Freiburg, Freiburg, Tyskland; og
3 Institut for Eksperimentel og Klinisk Farmakologi og Toksikologi, Det Medicinske Fakultet, Freiburg Universitet, Freiburg, Tyskland
Den beskyttende kardiovaskulære effekt af MRA'er blev først tilskrevet deres virkninger på diurese, blodvolumen og elektrolythomeostase.5 Men MR udtrykkes i flere celletyper og væv uden for nyrerne, og det er nu tydeligt, at MR i ekstrarenalt væv er en nøglefaktor bag sygdom (Figur 1).6,7 For mere end 20 år siden gav store kliniske forsøg bevis for, at MRA-behandling forbedrer dødelighed og sygelighed hos patienter med hjertesvigt med reduceret ejektionsfraktion (HFrEF), hvilket førte til en klasse IA-retningslinje. anbefaling.8-10 Siden da har en række eksperimentelle undersøgelser afsløret de cellulære og molekylære mekanismer, der ligger til grund for den gavnlige effekt på venstre ventrikel (LV) remodellering. Baseret på disse resultater er potentialet for MRA'er blevet evalueret i andre kardiovaskulære sygdomme, herunder koronararteriesygdom, arteriel hypertension, hjertesvigt med bevaret ejektionsfraktion (HFpEF), pulmonal hypertension (PH) og hjerteklapsygdom. Nærværende gennemgang opsummerer den nuværende viden om MR-aktivering og antagonisme ved hjerte-kar-sygdomme.
HFrEF og post-myokardieinfarkt remodeling MRA'er har etableret lægemidler til behandling af kronisk HFrEF, som påvist i flere undersøgelser.8 Eplerenone in Mild Patients Hospitalization and Survival Study in Heart Failure (EMPHASIS-HF) viste en reduktion i dødeligheden med 24 procent hos patienter med HFrEF og milde symptomer behandlet med eplerenon versus placebo.11 I Randomized Aldactone Evaluation Study (RALES) havde spironolacton en lignende effekt hos patienter med alvorlige hjertesvigtssymptomer, hvor dødeligheden var reduceret med 30 procent versus placebo.12 Studier har vist, at den ikke-steroide MRA-finerenon ligesom spironolacton og eplerenon reducerede niveauet af pro-B-type natriuretisk peptid (BNP) eller N-terminalt BNP (NT-proBNP) i fase II forsøg.13,14 Tidlig påbegyndelse af MRA-behandling i patienter med akut hjertesvigt viste sig at være sikre og veltolererede.15,16 Eplerenon forbedrede resultaterne for patienter med nedsat LV-funktion efter myokardieinfarkt (MI).1 7 Efterfølgende undersøgelser testede hypotesen om, at initiering af MR-blokade tidligt efter MI kunne forhindre hjerteombygning og forekomsten af hjertesvigt. Ved påbegyndelse inden for 72 timer efter symptomdebut forbedrede MRA-behandling BNP/NT-proBNP-niveauer hos patienter uden allerede eksisterende hjertesvigt.18 I en senere undersøgelse blev der imidlertid kun observeret en potentiel fordel ved tidlig MRA-behandling på kliniske resultater i undergruppen af højrisikopatienter med ST-elevation MI.19 En individuel metaanalyse på patientniveau af 3 store randomiserede kontrollerede forsøg med patienter med HFrEF viste også en 23 procent reduktion i pludselig hjertedød med MRA-behandling.20 Hos patienter med nyligt diagnosticeret HFrEF , var behandling med højere MRA-doser forbundet med overlegen forbedring af LV ejektionsfraktion ud over 3 måneder.21
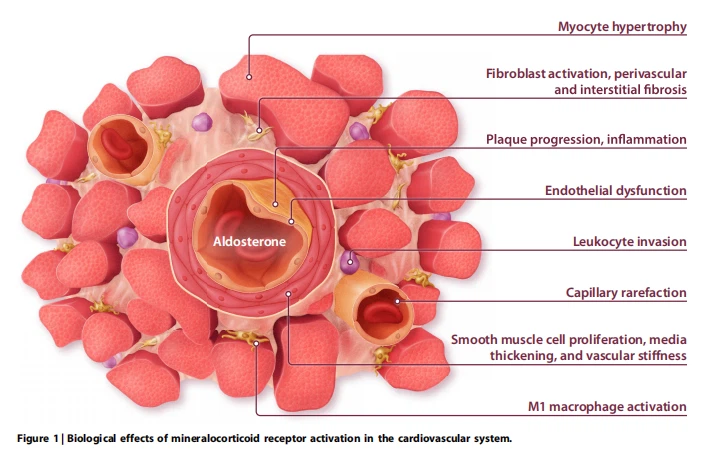
Eksperimentelle undersøgelser med MRA'er i dyremodeller af hjertesvigt og post-MI remodellering viste gavnlige effekter på hjertehypertrofi, fifibrose eller begge dele (figur 1).22-25 Efterfølgende gav brugen af musemodeller med cellespecifik MR-deletion bevis for, at disse virkninger blev medieret af MR-aktivering i kardiovaskulære celler. MR-deletion fra hjertemyocytter resulterede i mindre arstørrelse, mindre fifibrose af det fjerne væv og forbedret LV-funktion.26 Reduceret fifibrose efter iskæmisk skade var forbundet med svækket oxidativt stress og myocytapoptose, men højere antal neutrofiler og monocytter blev påvist i myokardiet væv fra MR-deficiente mus sammenlignet med vildtype-mus.26 Det er bemærkelsesværdigt, at MR-deletion fra myeloidceller ligeledes forbedrede LV-remodellering og inducerede et skift mod den mere reparative M2-makrofageundertype.27 MR-deletion fra glatte muskelceller (SMC'er) svækkede LV fifibrose, men havde mindre effekter på LV-funktionen.25 Dette indebærer, at MRA'er har effekter på forskellige celletyper, som synergistisk bidrager til skadeskontrol og heling efter MI.

Centraliteten af inflammation i at formidle den skadelige effekt af MR-aktivering er blevet bekræftet i modeller for kronisk hjertesvigt (figur 2). L-arginin methylester (L-NAVN)/angiotensin II infusion.28,29 Lignende virkninger blev observeret hos mus, der mangler MRS i T-celler.30 For ganske nylig blev SMC MR deletion vist at forbedre trykoverbelastningsinduceret LV hypertrofi, inflammation, fifibrose og dysfunktion.31 MR-deletion fra endotelceller eller hjertemyocytter forbedrede LV-funktionen, men i modsætning til iskæmisk skade regulerede den ikke fifibrose efter trykoverbelastning.32,33 Der blev ikke påvist nogen forskelle efter MR-deletion fra fibroblaster.32 Disse fund tyder på, at virkningen af MR på hjerteombygning afhænger af ikke kun celletypen, men også typen af skade.

Der er gjort en betydelig indsats for at dechifrere molekylære reguleringsmekanismer bag aldosteron/MR-induceret LV-ombygning. Velkarakteriserede inflammatoriske og fibrotiske effektormolekyler af MR i det kardiovaskulære system inkluderer galectin 3 (LGALS3) og lipocalin 2 (NGAL).55-58 Spændende nok, farmakologisk hæmning af modificeret citruspektin eller genetisk deletion af galectin 3-aldiosterone-aduceret kardiovaskulært svækket. remodeling.55,56 Plasmaniveauer af NGAL var positivt korreleret med cirkulerende aldosteronniveauer og fifibrose-biomarkører hos mennesker.57 Deletion af NGAL fra immunceller forhindrede LV-fifibrose som reaktion på aldosteroninfusion.58 Ligeledes forbedredes MR-deletion fra myeloide celler efter remodellering af hjerteceller. myokardieinfarkt, som var forbundet med reduceret NGAL-ekspression i kardiale makrofager.27 En nylig high-throughput-screening af mikroRNA'er identificerede miR-181a som en afgørende regulator af MR-signalering.59 miR-181en overekspression nedregulerede NGAL ekspression in vitro og in vivo og forbedret hjertefunktion i en MI-model af gnavere.59
HFpEF Forekomsten af HFpEF er stigende og udgør allerede mere end 50 procent af hjertesvigtstilfældene.60 Trods overlappende symptomer anses HFpEF for at være en separat enhed fra HFrEF.60 Sammenlignet med patienter med HFrEF er patienter med HFpEF ældre, flere ofte kvinder og overvægtige og har flere komorbiditeter, såsom diabetes og nyresygdom, der er forbundet med kronisk inflammation.60,61 MR-aktivering øger oxidativt stress og forringer nitrogenoxid (NO) signalering, hvilket fører til endotel dysfunktion, inflammation og perivaskulær fifibrosis.34 Selvom den ideelle prækliniske model til at studere HFpEF stadig mangler at blive defineret, er et klart fund, at MR-aktivering er forbundet med mange af de patofysiologiske træk, der karakteriserer HFpEF.62,63 MRA'er forbedrede diastolisk dysfunktion induceret af fedme, ovariektomi, nefrektomi, eller deoxycorticosteronacetat (DOCA)/salt hypertension hos mus.64-67 Celletypespecifik MR-deletion fra hjertemyocytter svækkes ed leukocytinvasion og fifibrose efter DOCA-behandling.68 I overensstemmelse med paradigmet for systemisk inflammation i HFpEF viste MR-deletion fra endotelceller eller myeloidceller den mest slående effekt på hjerteombygning (figur 2).35-38,54,69
Tidlige kliniske forsøg antydede de gavnlige virkninger af MRA'er hos patienter med HFpEF.70-72. Det var således uventet, at spironolacton ikke formåede at forbedre det sammensatte primære resultat af dødsfald som følge af kardiovaskulære årsager, aborteret hjertestop eller hospitalsindlæggelse for hjertesvigt i den store fase III Behandling af bevaret hjertesvigt med hjertesvigt med et forsøg med aldosteronantagonist (TOPCAT).73 Alvorlige betænkeligheder ved undersøgelsens udførelse sætter imidlertid spørgsmålstegn ved undersøgelsens gyldighed.74,75 I FINerenonen til reduktion af kardiovaskulær mortalitet og sygelighed ved diabetisk nyresygdom (FIG ARO-DKD) forsøg, reducerede den ikke-steroide MRA finerenon forekomsten af kardiovaskulære hændelser hos patienter med diabetisk nyresygdom,76 en patientgruppe med høj risiko for at udvikle HFpEF.60 Det er bemærkelsesværdigt, at den gavnlige virkning af finerenon overvejende var drevet af en lavere indlæggelsesrate for hjertesvigt, selvom patienter med allerede eksisterende HFrEF blev udelukket fra forsøget.76 To yderligere fase III kliniske forsøg, der sammenligner spironolacton (Spironolacton til behandling af hjertesvigt [SPIRIT-HF); NCT04727073; EudraCT 2017- 000697-11) og finerenon (Finerenone Trial to Investigate Efficacy and Safety Superior to Placebo in Patients with Heart Failure [FINEARTS-HF]; NCT04435626) med placebo hos patienter med hjertesvigt og mellemklasse eller bevaret ejektionsfraktion er pt. igangværende.

I Heart 'OMics' in aging (HOMAGE) forsøget reducerede spironolacton syntese og øget nedbrydning af type I kollagen og reducerede blodtryk, venstre forkammervolumen og BNP-niveauer hos personer med risiko for HFpEF.77 Om tidlig MRA-behandling kan forsinke forekomsten af hjertesvigt i sådanne populationer er endnu ikke fastlagt.
Åreforkalkning og koronararteriesygdom
Aterosklerose og koronararteriesygdom betragtes som kroniske inflammatoriske sygdomme78, og den stærke indflydelse af MR på vaskulær inflammation beskrevet ovenfor antyder en rolle for MR i deres patofysiologi. I apolipoprotein E knockout musemodellen forværrede aldosteroninfusion udviklingen af aterosklerose.79 Omvendt svækkede MRA'er inflammation og dannelse af reaktive oxygenarter, men forbedrede NO-biotilgængelighed og vaskulær funktion i fedmemodeller.80-83 Aldosteroneffekter på monocytrekruttering og plaqueenflammation hos mus, der mangler placenta vækstfaktor79 eller intercellulært adhæsionsmolekyle 1,84, hvilket indikerer en interaktion mellem endotelceller og monocytter i processen. In vitro fremmede MR ekspressionen af inflammatoriske molekyler i endotelceller og SMC'er.39,54,85-87 In vivo forbedrede MR-deletion fra endotelceller eller myeloidceller, men ikke fra SMC'er, vaskulær inflammation i musemodeller af aterosklerose.39 –41 Desuden øgede stimulering af monocytter med aldosteron inflammatorisk cytokinproduktion, afhængigt af opreguleringen af fedtsyresyntesevejen.88 Den voksende mængde litteratur om funktionen af myeloid celle MRS i medfødt immunitet og åreforkalkning er blevet opsummeret af van der Heijden et al. (2018).89 Bortset fra deres virkninger i åreforkalkning, gav MRA-behandling og MR-deletion fra SMC- eller myeloidceller gavnlige effekter på vaskulær ombygning efter mekanisk skade,42,43,90, hvilket indikerer en potentiel fordel ved MRA'er på postangioplastisk restenose. På trods af denne overbevisende eksperimentelle evidens er data fra kliniske forsøg på MRA'er i åreforkalkning stadig sparsomme.91 Det nylige forsøg med Finerenone in Reducing Kidney Failure and Disease Progression in Diabetic Kidney Disease (FIDELIO-DKD) viste for første gang, at behandling med den nye MRA finerenon kunne reducere forekomsten af MI hos patienter med diabetisk nyresygdom92, hvilket indikerer en potentiel rolle af MRA'er i den primære forebyggelse af kardiovaskulære hændelser.
Arteriel hypertension
Indvirkningen af aldosteron og MR på arteriel hypertension har været anerkendt i årtier. For eksempel øger aldosteroninfusion blodtrykket væsentligt hos uni-nephrektomiserede rotter, der får en kost med højt saltindhold.93,94 Ud over dets virkninger på Naþ og væskeretention, styrer aldosteron blodtrykket via MR i celler uden for nyrerne.95 Endotel MR aktivering inducerede produktionen af reaktive oxygenarter og forringede endotelafhængig vaskulær afslapning.44,80 Det er bemærkelsesværdigt, at disse effekter var mere udtalte hos hunmus sammenlignet med hanmus.96 MR-overekspression førte til en moderat stigning i blodtrykket.97 MR-deletion fra endotelceller ændrede ikke blodtrykket ved baseline eller som reaktion på stimulus,36,44,45,69, hvilket indikerer, at MR i endotelceller ved fysiologiske ekspressionsniveauer er uundværlig for blodtrykskontrol. I modsætning hertil peger adskillige undersøgelser på MRS i SMC'er som en nøgledeterminant for vaskulær stivhed og hypertension, især hos gamle mus (figur 2).46-48,98 Det blev foreslået, at MR via undertrykkelse af miR-155 øger ekspressionen og aktiviteten af L-type Ca2þ-kanaler i SMC'er, hvilket fører til en stigning i vaskulær tonus.46,47 Angiotensin II-induceret hypertension og efterfølgende organskade blev markant undertrykt af MR-deletion fra T-celler.49 Med hensyn til MRs rolle i myeloide celler, er der rapporteret delvist modstridende resultater på blodtryksresponset på DOC/salthypertension37 eller angiotensin II/L-NAME.29,38 Spironolacton viste sig at være effektiv hos patienter med resistent hypertension i flere kliniske forsøg og anbefales nu til patienter med vedvarende hypertension på trods af tredobbelt terapi.99.100 Den ikke-steroide MRA esaxerenon havde en effektivitet svarende til eplerenon til at sænke blodtrykket og er nu godkendt i Japan til behandling af essentiel hyperte nsion.101,102 I et nyligt fase 2b-forsøg var den ikke-steroide MRA KBP-5074 i stand til signifikant at sænke blodtrykket hos patienter med kronisk nyresygdom og ukontrolleret hypertension på trods af behandling inklusive en renin-angiotensin-systemhæmmer.103 I modsætning hertil patienter med kronisk nyresygdom og velkontrolleret hypertension, havde fifinerenon kun mindre yderligere virkninger på blodtrykket.76.104
PH og højre hjertesvigt
Forhøjede plasmaaldosteronniveauer er blevet observeret hos patienter med PH og hos mus efter eksponering for kronisk hypoxi, 50.105.106, hvilket antyder en rolle for MR i pulmonal vaskulær ombygning. Faktisk inducerer aldosteronstimulering PH-fænotyper in vivo og i dyrkede SMC'er eller endotelceller in vitro.50,107-109 MRA'er forbedrer vaskulær remodeling og højre ventrikelfunktion induceret af kronisk hypoxi eller monokrotalin i mus og rotter. i en pulmonal arterie banding-model, hvilket indebærer, at fordelene ved MRA'er på højre ventrikulær funktion indirekte kan forklares af den reducerede afterload.110 Eksperimentelle undersøgelser med mus med celletypespecifik MR-deletion afslørede, at den skadelige effekt af aldosteron på lungevaskulaturen medieres af MR i endotelceller i stedet for SMC'er, fibroblaster eller makrofager (figur 2).50 Genekspressionsanalyser og in vitro undersøgelser peger på en interaktion mellem endotelceller og andre celletyper i processen, der involverer endotelin{{13 }} signalvej og parakrin krydstale via exosomer.50,108,109,111 En post hoc analyse fra Ambrisentan for the Treatment af pulmonal arteriel hypertension (ARIES) 1 og 2-forsøg tydede på en gavnlig virkning af spironolacton, når den blev tilføjet til endotelin-1-receptorantagonisten ambrisentan hos patienter med PH.112. Der er pt. igangværende (NCT01712620).

Potentielle fremtidige retninger Viden om MR-effekter ved hjerte-kar-sygdomme udvides fortsat, hvilket peger på nye potentielle indikationer for MRA. Tilgængeligheden af nye, ikke-steroide MRA'er kan yderligere udvide spektret af indikationer og muliggøre klinisk brug af MRA'er i højrisikopatientpopulationer.4 Prækliniske og tidlige kliniske data tyder på, at MRA'er kan være effektive til at forhindre kemoterapi-induceret kardiotoksicitet, en relevant bivirkning af anticancer-lægemidler, der fører til LV-svigt, hos kvindelige patienter.51.113.114 Derudover indikerer voksende evidens, at MR-aktivering forårsager uønsket ombygning af ikke kun ventriklerne, men også atrierne. Patienter med primær aldosteronisme har højere risiko for at udvikle atrieflimren sammenlignet med patienter med essentiel hypertension.115 Spændende nok blev atriefibrose induceret af transformation af vækstfaktor b svækket af MR-deletion i osteoblaster (Figur 2).52 I forskellige eksperimentelle modeller reducerede MRA'er atriefifibrose og dermed byrden af atrieflimren,116-118, hvilket tyder på en potentiel fordel ved MRA'er hos patienter med atrieflimren. I overensstemmelse med denne mulighed afslørede en metaanalyse af kliniske forsøg en væsentlig reduktion i forekomsten af atrieflimren hos MRA-behandlede patienter sammenlignet med kontrolgrupper.119
Mitral regurgitation er en almindelig hjerteklaplidelse, der ofte er forbundet med strukturel forringelse og en forstyrret ekstracellulær matrix af mitralklapbladene.120 Nyere beviser tyder på, at aldosteron ved at aktivere MR driver proteoglycanproduktionen af interstitielle celler og endotel-til-mesenkymal overgang i mitralklapper.53 Hos mus svækkede MRA-behandling eller MR-deletion i endotelceller mitralklapombygningen.53 Denne effekt blev ledsaget af nedsat ekspression af fibrotiske markører i LV-væv hos mus behandlet med spironolacton.121 Selvom det i øjeblikket er begrænset til interventionel eller kirurgisk reparation, MRA'er kan således repræsentere en ny behandlingsmulighed for mitralregurgitation.6.120
Konklusioner
Beviser samler sig fra en række eksperimentelle undersøgelser, der viser, at Mrs i hjertemyocytter, endotelceller, SMC'er, myeloidceller, T-celler og osteoblaster har en direkte indvirkning på hjertesvigt og andre kardiovaskulære sygdomme. Afhængigt af typen af sygdom eller stimulus har forskellige celletyper MRS med forskellige funktioner, der bidrager til nettoeffekten af inflammation og fifibrose efter aktivering. Den tilgængelige indsigt diskuteret i denne gennemgang vil danne grundlag for yderligere udvikling og evaluering af klassiske og nye MRA'er for yderligere kardiovaskulære indikationer.
REFERENCER
1Lother A, Moser M, Bode C, et al. Mineralokortikoider i hjertet og vaskulaturen: ny indsigt for gamle hormoner. Annu Rev Pharmacol Toxicol. 2015;55:289-312.
2. Shibata S. 30 år af mineralocorticoid receptoren: mineralocorticoid receptor og NaCl transportmekanismer i den renale distale nefron. J Endocrinol. 2017;234:T35–T47.
3. Kolkhof P, Barfacker L. 30 år af mineralocorticoid-receptoren: mineralocorticoid-receptorantagonister: 60 års forskning og udvikling. J Endocrinol. 2017;234:T125–T140.
4. Agarwal R, Kolkhof P, Bakris G, et al. Steroide og ikke-steroide mineralokortikoidreceptorantagonister i kardiorenal medicin. Eur Heart J. 2021;42:152–161.
5. Struthers AD. Hvorfor forbedrer spironolacton dødeligheden ud over en ACE-hæmmer ved kronisk hjertesvigt? Br J Clin Pharmacol. 1999;47:479-482.
6. Lother A. Mineralocorticoid-receptorer: masterregulatorer af ekstracellulær matrix-ombygning. Circ Res. 2020;127:354-356.
7. Bauersachs J, Jaisser F, Toto R. Mineralocorticoid receptor aktivering og mineralocorticoid receptor antagonist behandling i hjerte- og nyresygdomme. Forhøjet blodtryk. 2015;65:257-263.
8. Ponikowski P, Voors AA, Anker SD, et al. 2016 ESC-retningslinjer for diagnosticering og behandling af akut og kronisk hjertesvigt: Task Force for diagnose og behandling af akut og kronisk hjertesvigt af European Society of Cardiology (ESC). Udviklet med det særlige bidrag fra Heart Failure Association (HFA) i ESC. Eur Heart J. 2016;37:2129–2200.
9. Berliner D, Hanselmann A, Bauersachs J. Behandlingen af hjertesvigt med reduceret ejektionsfraktion. Dtsch Arztebl Int. 2020;117:376-386.
10. Lother A, Hein L. Farmakologi af hjertesvigt: fra grundlæggende videnskab til nye terapier. Pharmacol Ther. 2016;166:136-149.
11. Zannad F, McMurray JJ, Krum H, et al. Eplerenon hos patienter med systolisk hjertesvigt og milde symptomer. N Engl J Med. 2011;364: 11-21.
12. Pitt B, Zannad F, Remme WJ, et al. Effekten af spironolacton på morbiditet og dødelighed hos patienter med alvorligt hjertesvigt. Randomized Aldactone Evaluation Study investigators. N Engl J Med. 1999;341:709-717.
13. Pitt B, Kober L, Ponikowski P, et al. Sikkerhed og tolerabilitet af den nye ikke-steroide mineralocorticoid-receptorantagonist BAY 94-8862 hos patienter med kronisk hjertesvigt og mild eller moderat kronisk nyresygdom: et randomiseret, dobbeltblindt forsøg. Eur Heart J. 2013;34:2453–2463.
14. Filippatos G, Anker SD, Bohm M, et al. En randomiseret kontrolleret undersøgelse af fifinerenon vs. eplerenon hos patienter med forværret kronisk hjertesvigt og diabetes mellitus og/eller kronisk nyresygdom. Eur Heart J. 2016;37:2105–2114.
15. Butler J, Anstrom KJ, Felker GM, et al. Effekt og sikkerhed af spironolacton ved akut hjertesvigt: ATHENA-HF randomiseret klinisk forsøg. JAMA Cardiol. 2017;2:950-958.
16. Asakura M, Ito S, Yamada T, et al. Effekt og sikkerhed ved tidlig påbegyndelse af Eplerenon-behandling hos patienter med akut hjertesvigt (TIDLIGERE forsøg): et multicenter, randomiseret, dobbeltblindt, placebokontrolleret forsøg. Eur Heart J Cardiovasc Pharmacother. 2022;8:108-117.
17. Pitt B, Remme W, Zannad F, et al. Eplerenon, en selektiv aldosteronblokker, hos patienter med venstre ventrikulær dysfunktion efter myokardieinfarkt. N Engl J Med. 2003;348:1309-1321.
18. Montalescot G, Pitt B, Lopez de Sa E, et al. Tidlig eplerenonbehandling hos patienter med akut ST-elevation myokardieinfarkt uden hjertesvigt: Randomized Double-Blind Reminder Study. Eur Heart J. 2014;35:2295–2302.
19. Beygui F, Cayla G, Roule V, et al. Tidlig aldosteronblokade ved akut myokardieinfarkt: ALBATROSS randomiserede kliniske forsøg. J Am Coll Cardiol. 2016;67:1917-1927.
20. Rossello X, Ariti C, Pocock SJ, et al. Virkning af mineralocorticoid-receptorantagonister på risikoen for pludselig hjertedød hos patienter med hjertesvigt og venstre ventrikulær systolisk dysfunktion: en individuel metaanalyse på patientniveau af tre randomiserede kontrollerede forsøg. Clin Res Cardiol. 2019;108:477-486.
21. Duncker D, Konig T, Hohmann S, et al. Undgå utidig implantation af cardioverter/defibrillator ved intensiveret optimering af hjertesvigtsterapi understøttet af den bærbare cardioverter/defibrillator – PROLONG-undersøgelsen. J Am Heart Assoc. 2017;6:e004512.
22. Kuster GM, Kotlyar E, Rude MK, et al. Mineralocorticoid-receptorhæmning forbedrer overgangen til myokardiesvigt og mindsker oxidativt stress og inflammation hos mus med kronisk trykoverbelastning. Cirkulation. 2005;111:420-427.
23. Fraccarollo D, Galuppo P, Schmidt I, et al. Additiv forbedring af venstre ventrikulær ombygning og molekylære ændringer ved kombineret aldosteron- og angiotensinreceptorblokade efter myokardieinfarkt. Cardiovasc Res. 2005;67:97-105.
24. Fraccarollo D, Galuppo P, Schraut S, et al. Øjeblikkelig mineralocorticoid receptorblokade forbedrer myokardieinfarktheling ved modulering af det inflammatoriske respons. Forhøjet blodtryk. 2008;51:905-914.
25. Gueret A, Haruki N, Favre J, et al. Vaskulær glatmuskel mineralocorticoid receptor bidrager til koronar og venstre ventrikulær dysfunktion efter myokardieinfarkt. Forhøjet blodtryk. 2016;67:717-723. 26. Fraccarollo D, Berger S, Galuppo P, et al. Sletning af kardiomyocytmineralkortikoidreceptor forbedrer uønsket ombygning efter myokardieinfarkt. Cirkulation. 2011;123:400-408.
27. Fraccarollo D, Thomas S, Scholz CJ, et al. Makrofag mineralocorticoid receptor er en pleiotrop modulator af myokardieinfarktheling. Forhøjet blodtryk. 2019;73:102-111.
28. Li C, Zhang YY, Frieler RA, et al. Myeloid mineralocorticoid receptormangel hæmmer aortakonstriktion-induceret hjertehypertrofi hos mus. PLoS One. 2014;9:e110950.
29. Usher MG, Duan SZ, Ivaschenko CY, et al. Myeloid mineralocorticoid receptor kontrollerer makrofagpolarisering og kardiovaskulær hypertrofi og remodellering hos mus. J Clin Invest. 2010;120:3350-3364.
30. Li C, Sun XN, Zeng MR, et al. Mineralocorticoid-receptormangel i T-celler dæmper trykoverbelastningsinduceret hjertehypertrofi og dysfunktion gennem modulerende T-celleaktivering. Forhøjet blodtryk. 2017;70:137-147.
31. Kim SK, Biwer LA, Moss ME, et al. Mineralocorticoid receptor i glat muskulatur bidrager til trykoverbelastningsinduceret hjertesvigt. Circ hjertesvigt. 2021;14:e007279.
32. Lother A, Berger S, Gilsbach R, et al. Ablation af mineralocorticoid-receptorer i myocytter, men ikke i fibroblaster, bevarer hjertefunktionen. Forhøjet blodtryk. 2011;57:746-754.
33. Salvador AM, Moss ME, Aronovitz M, et al. Endothelial mineralocorticoid receptor bidrager til systolisk dysfunktion induceret af trykoverbelastning uden at modulere hjertehypertrofi eller inflammation. Physiol Rep. 2017;5:e13313.
34. Lother A, Hein L. Vaskulære mineralokortikoidreceptorer: forbinder risikofaktorer, hypertension og hjertesygdomme. Forhøjet blodtryk. 2016;68:6–10.
35. Jia G, Habibi J, DeMarco VG, et al. Endothelial mineralocorticoid receptor deletion forhindrer diæt-induceret hjertediastolisk dysfunktion hos kvinder. Forhøjet blodtryk. 2015;66:1159-1167.
36. Rickard AJ, Morgan J, Chrissobolis S, et al. Endotelcellemineralkortikoidreceptorer regulerer deoxycorticosteron/saltmedieret hjerteomdannelse og vaskulær reaktivitet, men ikke blodtryk. Forhøjet blodtryk. 2014;63:1033-1040.
37. Rickard AJ, Morgan J, Tesch G, et al. Deletion af mineralocorticoid-receptorer fra makrofager beskytter mod deoxycorticosteron/salt-induceret hjertefifibrose og forhøjet blodtryk. Forhøjet blodtryk. 2009;54:537-543.
38. Bienvenu LA, Morgan J, Rickard AJ, et al. Makrofag mineralocorticoid receptor signalering spiller en nøglerolle i aldosteron-uafhængig hjertefifibrose. Endokrinologi. 2012;153:3416-3425.
39. Moss ME, Lu Q, Iyer SL, et al. Endotheliale mineralocorticoid-receptorer bidrager til vaskulær inflammation i åreforkalkning på en kønsspecifik måde. Arterioscler Thromb Vasc Biol. 2019;39:1588-1601.
40. Shen ZX, Chen XQ, Sun XN, et al. Mineralokortikoid receptormangel i makrofager hæmmer åreforkalkning ved at påvirke skumcelledannelse og efferocytose. J Biol Chem. 2017;292:925-935.
41. Moss ME, DuPont JJ, Iyer SL, et al. Ingen signifikant rolle for glatmuskelcelle-mineralkortikoidreceptorer i åreforkalkning i apolipoprotein-E knockout-musemodellen. Front Cardiovasc Med. 2018;5:81.
for flere oplysninger:Ali.ma@wecistanche.com
