Integrering af CKD i amerikansk primærpleje: bygge bro mellem viden og implementeringshuller
May 23, 2023
Abstrakt
Kronisk nyresygdom (CKD) påvirker 37 millioner amerikanske voksne, som oplever høje forekomster af kardiovaskulære hændelser og er i risiko for nyresvigt og dødelighed. Rutinemæssig konstatering af tilfælde i primærpleje for CKD med estimeret glomerulær filtrationshastighed (eGFR) og urinalbumin-kreatinin-forhold (uACR) bør fokusere på risikotilstande, især diabetes, hypertension og kardiovaskulær sygdom, som anbefalet af retningslinjer for klinisk praksis. Diagnosen CKD er forbundet med mange vigtige aspekter af pleje, herunder patientbevidsthed, patientengagement og forbedret implementering af evidensbaserede interventioner. Individualiseret pleje, der skræddersyer CKD-interventioner proportionalt med den negative udfaldsrisiko eller eGFR- og uACR-varmekortet, er en stor udfordring for primær CKD-pleje, fordi tilstanden er heterogen med hensyn til både årsagen og sværhedsgraden. Den koordinerede plejetilgang til CKD-håndtering er nødvendig for at implementere bedste praksis inden for kronisk sygdomshåndtering, der involverer det tværfaglige team. Et integreret system understøtter den tidsbegrænsede primære kliniker med CKD-registreringsfunktioner, kliniske beslutningsstøtteværktøjer, kvalitetsforbedringsinitiativer og betalingsmodelincitamenter for at fremme en reduktion i uønskede resultater og indeslutning af udgifter. En CKD-befolkningssundhedsstrategi kan bygges til at adressere undervisning i primærpleje og implementeringshuller ud fra perspektiverne af test, påvisning af sygdom, interventioner og koordineret systemintegreret pleje. Registerfunktion og dataovervågning af CKD-byrden, leveringsinterventioner og resultater er nøglefunktioner. Implementering af de Race-free 2021 CKD-(Epidemiology Collaboration) EPI eGFR-rapporteringsanbefalinger ved at engagere lokale nefrologiske, administrative, kliniske laboratorie- og sundhedsmæssige ledere bør hjælpe med at drive strategien for befolkningens sundhedsdesign og datavurderingen.

Klik her for at fåfordelene ved Cistanche
Introduktion
Ifølge Centers for Disease Control and Prevention påvirker CKD 37 millioner amerikanske voksne, som oplever høje forekomster af kardiovaskulære hændelser og er i risiko for nyresvigt. Dødelighed er underanerkendt som en konkurrerende begivenhed versus nyresygdom i slutstadiet (ESKD). Den oprindelige definition og stratificering af CKD, offentliggjort i 2002 af US Kidney Disease Outcomes Quality Initiative, ændrede klinisk praksis på verdensplan, og fremmede vedtagelsen af eGFR-rapportering i stedet for serumkreatinin alene og præsenterede muligheder for nyresygdomsgenkendelse og -håndtering i den primære sundhedspleje. The International Kidney Disease: Improving Global Outcomes 2012 Clinical Practice Guideline for CKD Evaluation and Management, godkendt i USA af Kidney Disease Outcomes Quality Initiative, opdaterede det tidligere arbejde baseret på epidemiologi, herunder mere end 1 million patienter for at beskrive en årsag-glomerulær filtration rate-albuminuri (CGA) CKD definition og klassificering for at stratificere risiko baseret på eGFR og uACR.
Desværre afslører en nylig evaluering af pleje på amerikansk befolkningsniveau for personer med eGFR under 60 ml/min pr. 1,73 m2, at cirka 40 procent modtager uACR-test, kun 12 procent til 20 procent har tegn på en CKD-diagnose, mindre end 50 procent har kontrolleret hypertension, 40 procent har kontrolleret diabetes, 29 procent til 31 procent bruger statiner til at reducere kardiovaskulære hændelser, mindre end 50 procent behandles med angiotensin-konverterende enzymhæmmer (ACEi) eller angiotensinreceptorblokker (ARB),6 og nefrologiske tjenester er leveret til kun cirka 50 procent af patienter med CKD G4 og G5. Selvom disse data overvejende repræsenterer levering i primærpleje, skal nefrologisk forberedelse til nyreerstatningsterapi i USA forbedres, hvilket afspejles blandt dem med ESKD ved brug af hæmodialysekateter hos mere end 80 procent af patienterne ved påbegyndelse af hæmodialyse og lave rater af både hjemmedialyse og præ -emptiv nyretransplantation.
Nyresundhedsuligheder efter race og etnicitet er komplekse med flere bidragydere, men disse er blevet dokumenteret i den medicinske litteratur i det mindste siden 1980'erne. Undersøgelser har afsløret forskelle i sundheds- og sundhedsydelser, som uforholdsmæssigt påvirker afroamerikanere sammenlignet med ikke-spansktalende hvide individer, med næsten dobbelt så stor forekomst af hypertension, der forårsager eller bidrager til CKD, ca. gange forekomsten af ESKD og mindre brug af patient- centriske nyreerstatningsterapier, hjemmedialyse og nyretransplantation. Hispanics, asiater, hawaiianere, stillehavsøboere og amerikanske indianere har også dokumenteret nyresundhedsforskelle med nuancer på tværs af grupperne. Årsagerne til observerede uligheder er multifaktorielle, men de kan især tilskrives sociale determinanter for sundhed. Som en del af USA's opgør med race og etnicitet i samfundet er ubevidste klinikere og institutionaliseret racisme i sundhedsvæsenet i stigende grad blevet anerkendt som bidragydere til uligheder i nyresundheden.
Desværre er der uønskede direkte virkninger som følge af COVID-19-pandemien blandt sorte og latinamerikanske amerikanere sammenlignet med ikke-spansktalende hvide personer, herunder dramatisk højere frekvenser af hospitalsindlæggelse, akut nyreskade og død. Indirekte pandemiske virkninger i den uinficerede befolkning er reducerede kliniske møder, øgede huller i pleje, lavere frekvenser af CKD laboratorieovervågning og færre medicinrefill for kardiometaboliske CKD-risikotilstande sammenlignet med historiske kontroller.
Der er betydelig plads til forbedringer i behandlingen af personer med CKD af både primære klinikere og specialister. Denne korte gennemgang vil tage fat på undervisning i primærpleje og implementeringshuller i CKD ud fra perspektiverne af testning, påvisning af sygdom, interventioner til håndtering, tværfaglig pleje og koordineret systemintegreret pleje, som kun er nyt, da det foreslår inkorporering af Racefree 2021 eGFR-rapporteringsanbefalinger og moderne amerikansk sundhed equity momentum i tilgangen.

Cistanche kosttilskud
Primærpleje Implementering af CKD-test
Routine primary care case finding for CKD with eGFR and uACR should focus on risk conditions, particularly; diabetes, hypertension, cardiovascular disease, and a family history of kidney disease, as recommended by clinical practice guidelines from the American Diabetes Association, Kidney Disease: Improving Global Outcomes, Kidney Disease Outcomes Quality Initiative, and other organizations, in contrast to mass or general population screening. In recent years in the United States, annual uACR testing is approximately 40% for diabetes and less than 10% for hypertension in national data sets from Medicare, commercial insurance, health systems, and clinical laboratories, supporting the need for interventions to improve targeted albuminuria testing. There are some challenges for clinicians to order uACR because laboratories do not universally offer the test and reporting formats vary, introducing inconsistencies and complexity in the interpretation of the results. For example, some laboratories only offer the urinary albumin concentration test without offering the ratio. Finally, clinicians are unlikely to order tests that they are not sure how to interpret, suggesting low rates of albuminuria testing may simply reflect an underappreciation of the utility of the results or challenges in the interpretation. Testing and recognition of albuminuria will inform the selection of patients who need additional interventions beyond the current ACEi or ARB paradigm, including novel kidney- and cardiovascular-protective therapies, such as sodium-glucose cotransporter-2 inhibitor (SGLT-2i), glucagonlike peptide-1 receptor agonists (GLP1 RA) in type 2 diabetes, and the non-steroidal mineralocorticoid inhibitor (finer enone) in type 2 diabetes. Nephrotic albuminuria or the uACR of approximately >2000 mg/g er vigtigt for primære klinikere at erkende som tyder på en glomerulær sygdomsårsag, der kan være uafhængig af diabetes eller hypertension som en komorbiditet, der kræver nefrologisk konsultation. Primærplejeuddannelsen bør også gennemgå yderligere diagnostiske tests for at identificere årsagen og en mulig indikation for nefrologisk konsultation for usikkerhed om eGFR-fortolkning.
Data tyder på, at klinikere tester eGFR meget oftere end uACR med årlige rater på 80 procent til 90 procent af befolkningen med risiko for diabetes eller hypertension. College of American Pathologists internationale prøve afslørede, at 92 procent af laboratorierne rapporterede eGFR i 2019, med de fleste af de undersøgte laboratorier i Nordamerika. Laboratorieinkludering af eGFR-rapportering med de allestedsnærværende sæt kaldet de grundlæggende og omfattende metaboliske og nyrefunktionspaneler for at bidrage til den bredere anvendelse af nyrefiltreringsblodprøven. Indtil for nylig anbefalede eGFR-rapportering brugen af 2009 CKD-EPI-samarbejdet eGFRcr-ligningen med og uden en afroamerikansk koefficient, hvilket komplicerer den kliniske vurdering af eGFR. Udfordringerne ved at tildele race i rutinemæssig praksis, de samfundsmæssige bekymringer om at antyde en biologisk årsag til en social konstruktion og de fyldte spørgsmål om racisme i medicin blev elegant gennemgået af Darshali Vyas i en indflydelsesrig leder. Brugen af 2021 CKD-EPI eGFRcreller eGFRCR-CYSløser disse mangler.
Primary Care CKD-detektion
Diagnosen CKD er forbundet med mange vigtige aspekter af pleje, herunder patientbevidsthed, patientengagement og forbedret implementering af evidensbaserede interventioner. Påvisning af CKD ved hjælp af CKD-diagnosekoder forbliver lav i praksis i primærpleje, selvom diagramgennemgang eller naturlig sprogbehandlingsanalyse mere præcist afspejler klinikerens diagnose. ADD-CKD-undersøgelsen af mere end 9 tusinde amerikanske patienter med type 2-diabetes administreret af 466 primære klinikere afslørede CKD-detektion hos kun 12 procent af befolkningen med laboratoriebevis for tilstanden. Det er vigtigt, at bevidstheden eller selvrapporteret CKD var 81,1 procent med praktiserende læge versus 2,6 procent i fravær af en diagnose. Bevidsthed er det første skridt til at øge patientengagement og selvledelse. Adskillige undersøgelser har afsløret en variabel, men generelt positiv sammenhæng mellem påvisning af CKD og forbedret implementering af evidensbaserede interventioner.

Herba Cistanche
Primærplejeinterventioner i forhold til CKD-risikoen
Individualiseret pleje, der skræddersyer CKD-interventioner proportionalt med den negative udfaldsrisiko eller eGFR- og uACR-varmekortet, er en stor udfordring for primær CKD-pleje, fordi tilstandene er heterogene med hensyn til årsag og sværhedsgrad. CKD er en heterogen tilstand, således at personer med kun lidt lavt estimeret GFR uden forhøjet uACR kan have kun små håndteringsmæssige og prognostiske implikationer, mens personer med meget lav estimeret GFR og/eller alvorligt forhøjet uACR kan have kritisk risiko for uønskede hændelser og kræver rettidig tværfaglige interventioner for at imødegå den betydelige risiko for hospitalsindlæggelse, kardiovaskulære hændelser, nyresvigt og dødelighed. Kontroversen om skelnen mellem tab af eGFR med normal aldring og CKD blandt seniorer med eGFR 45 til 60 ml/min pr. 1,73 m2i fravær af albuminuri (CKD G3aA1) er bemærkelsesværdig. Områder til overvejelse i denne indstilling ville være den potentielle rolle af cystatin C-testning for at hjælpe med at stratificere risiko med mere nøjagtige eGFRcr-cys eller 2012 CKD-EPI eGFRcys. Konsekvenser af CKD G3aA1 hos seniorer omfatter patientmedicineringssikkerhedsfaktorer, kardiovaskulær risiko, kognitive svækkelsesrisici og risici for større operation perioperativ akut nyreskade, herunder mangel på beviser til støtte for ACEi eller ARB og SGLT{{7}, jeg bruger til nyre risikoindikationer.
Vigtige interventioner til behandling af kronisk nyreinsufficiens i primærpleje omfatter hypertension kontrolmål individualiseret i et område, der generelt bør være mindre end 130/80 mm Hg med højt motiverede patienter med den højeste kardiovaskulære risiko, der tilbydes en<120 mm Hg systolic target and targets 140/90 mm Hg or even higher for patients with or at risk for complications of intensive targets such as hemodynamic acute kidney injury or falls. Similarly, diabetes control should be individualized in a range of less than 7% as the general recommendation.
Nyre- og hjertebeskyttende medicin, ACEi eller ARB, SGLT-2i, GLP-1 RA og ikke-steroid mineralokortikoidhæmmer (finere enon), bør anvendes til risikopopulationen baseret på nylige randomiserede forsøg. Kardiovaskulære trombotiske hændelser, hjertesvigt og kardiovaskulær dødelighed bør fremhæves som beriget i henhold til eGFR- og uACR-risikostratificeringen. Reduktion af kardiovaskulær risiko er derfor vigtig at understrege med statin-baseret behandling for at reducere akutte trombotiske hændelser og særlige indgreb i hjertesvigt, der ud over ACEi eller ARB og SGLT-2i kan omfatte betablokkere, neprilysinhæmmere, og diuretikabehandlinger.
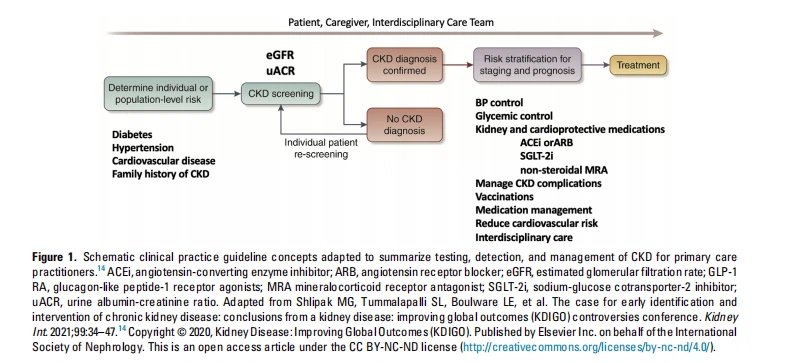
Årlige vaccinationer for influenza (almindelig dosis eller høj dosis for personer på 65 år og ældre) og pneumokokvaccinationsserien er bevisbaserede, ikke kun for at reducere infektionsrelaterede hospitalsindlæggelser og dødelighed, men også forbundet med efterfølgende reduktioner i kardiovaskulær indlæggelse, der kan være relateret til mindre mikroinflammation af endotelet i den vaccinerede CKD-population. Selvom der indsamles analoge data, er COVID-19-vaccination en vigtig moderne CKD-intervention for at reducere hospitalsindlæggelse og dødsrisiko. Medicinhåndtering, der overvejer eGFR, er vigtig for at forhindre akut nyreskade, hypoglykæmi og andre patientsikkerhedsrisici. Udbredelse af destilleret klinisk praksis retningslinjekoncepter, der ville være lettere at bruge i primær pleje (Figur 1), er vigtig for implementeringen for at forbinde testprocessen med evidensbaserede interventioner.
CKD koordineret tværfaglig pleje
Den koordinerede plejetilgang til CKD-håndtering er nødvendig for at implementere bedste praksis inden for kronisk sygdomshåndtering, der udnytter det tværfaglige team, herunder, men ikke begrænset til, den praktiserende læge, diætist, farmaceut, endokrinolog, kardiolog, nefrolog, mental sundhedsprofessionel og socialrådgiver. En ideel ramme omfatter yderligere 2 to teammedlemmer i nærheden på et klinisk sted, hvor patienterne drager fordel af håndteringen af deres komorbiditeter og livsstilsændringer gennem patientengagement og uddannelse på en optimeret strømlinet måde. Den multidisciplinære koordinerede tilgang har afsløret lovende langsommere fald i eGFR, øget blodtryk og diabeteskontrol, øge leveringen af CKD-interventioner, reducere hospitalsindlæggelse, øge brugen af arteriovenøs fistel og øge andelen af ambulant dialyseinitiering, der forbedrer sygeligheden og indeholder udgifter.
Medicinsk ernæringsterapi (MNT) fortjener særlig vægt for CKD, da det er meget underudnyttet i rutinepraksis. Medvirkende faktorer inkluderer lave frekvenser af henvisninger fra klinikere, refusionsbegrænsninger og lav adgang til erfarne registrerede diætister og diabetespædagoger. Dette på trods af sammenhænge med bedre risikofaktorkontrol af hypertension og diabetes, svækkelse af tab af eGFR og forbedring af resultaterne for de patienter, der påbegynder dialyse året efter at have fået MNT. Sammenligninger med patienter, der ikke får MNT, kræver risikojustering, og virkningen vil sandsynligvis variere. Ikke desto mindre er MNT også en vigtig potentiel intervention for at imødegå sundhedsforskelle i fødevaresikkerhed for patienter, der kan opholde sig i fødevareørkener eller fødevaresumpe, hvor adgangen til sunde kostvalg er begrænset.
Primærplejeklinikere identificerer også barrierer for nefrologisk CKD co-management, hvilket resulterer i en forstyrrelse i plejekontinuummet. Uklare roller og ansvarsområder, begrænset kommunikation og variabel adgang til nefrologer kan overvindes ved samarbejde med en lille gruppe nefrologer, en informationsudveksling med fokus på at udvælge nefrologer, der kommunikerer effektivt og/eller bruger den samme elektroniske patientjournal som den primære læge, og brug af en elektronisk nefrologisk konsultationsplatform i udvalgte tilfælde. Systematisk uddannelse og interventioner lover at hjælpe den primære kliniker med at henvise selektivt ved hjælp af koordineret pleje inden for det tværfaglige team.
Systemintegreret CKD-pleje
Systemintegreret pleje vil være nøglen til at støtte primære klinikere i sammenhæng med tidsbegrænsninger for at opnå den dristige 25 procents reduktion i forekomsten af ESKD inden 2030 af Advancing American Kidney Health Initiative Executive Order. CKD Intercept primærplejeklinikers engagement fra National Kidney Foundation omfatter et Laboratory Engagement Initiative for at forenkle bestilling af primære klinikere af nyretest og en harmoniseret nyresygdom: Improving Global Outcomes 2012 rapporteringsplan for de test, der er defineret af nyreprofilen (eGFR og uACR) som er blevet anerkendt af US Choosing Wisely-initiativet. Implementering af racefri eGFR-rapportering som anbefalet af National Kidney Foundation-American Society of Nephrology Task Force endelige rapport for primærplejebefolkningens sundhed bør omfatte samarbejde med kliniske laboratorier, nefrologiske kliniske ledere og sundhedslighedseksperter for at sikre, at 2021 CKD-EPI eGFRcr rapporteres og fortolkes korrekt. Systematisk indsats letter øget, rutinemæssig og udvalgt brug af cystatin C til at bekræfte eGFR hos voksne, der er i risiko for eller har CKD, fordi kombination af rutinemæssige nyrefiltreringsmarkører er mere nøjagtige og ville understøtte bedre kliniske beslutninger end hver enkelt markør alene ved at bruge 2021 CKD -EPI eGFRcr-cys eller 2012 CKD-EPI eGFRcys, der også er racefri. Implementering af systematiske validerede vurderinger såsom social deprivation-indekset vil hjælpe med at flytte primære klinikere væk fra race og etnicitet som CKD-risikotilstande til alternativt at fokusere på sociale determinanter for sundhed, primært og sekundært på genetisk afstamning, som er en biologisk konstruktion. F.eks. kan APOL-1 genetisk testning tilbydes til personer med eller i risiko for CKD, som frivilligt selv rapporterer vestafrikansk genetisk afstamning. Race og etnicitet skal fortsætte med at blive brugt på befolkningsniveau på en frivillig, gennemsigtig og kulturelt følsom måde til dataindsamling for at evaluere sundhedslighed i CKD-befolkningssundhedsinterventioner.
National Kidney Foundation Change Package skitserer trin til opbygning af en strategi for CKD befolkningssundhed, der begynder med dataindsamling for at identificere virkningen af CKD i sundhedssystemet med involvering af lederskab, der kan omfatte klinisk, klinisk laboratorium, datavidenskab, administrativ og sundhedsaktører og forkæmpere. De næste trin efter at have indkaldt disse er at definere CKD-interventionen, bruge data til at fremme forbedringer, der bør informere primærplejefaglig uddannelse og identificere huller i plejen gennem kortsigtede kvalitetsforbedringscyklusser. En del af den primære sundhedsuddannelse bør omfatte, hvordan man uddanner og engagerer patientpopulationen. Resultater af interesse på længere sigt kunne omfatte ændringer i overgangene mellem CKD G-stadier, ændringer i hændelsen og den udbredte ESKD-population, indvirkning på kardiovaskulære komplikationer og omkostningsimplikationer. En overordnet tilgang til overvågning af befolkningssundhedsdata om indvirkning på sundhedslighed bør understreges på tværs af interessenter og ledere.

Cistanche ekstrakt
Kvalitetsforbedring
Kvalitetsforbedrende foranstaltninger og målinger har brug for yderligere udvikling for CKD befolkningens sundhed. National Kidney Foundation udviklede også Kidney Health Evaluation for personer med diabetes for at sikre, at elektroniske kliniske kvalitetsmålinger for eGFR- og uACR-testformidling implementeres i kommercielle sygeforsikringsplaner i USA af National Committee for Quality Assurance. Forfining af en platform af foranstaltninger til at bygge videre på denne foranstaltning til forbedring af primærplejekvaliteten og implementering af betalingsmodeller er i gang.
Kvalitetsforbedringsinitiativer bør fokusere på den samlede patientcyklus af planlægning før besøg, kontorbesøg og behandling efter besøg. Optimering af patientpleje for CKD-patienter omfatter følgende: (i) uddannelse af teammedlemmerne, patienten og plejepersonalet, der fremhæver målene for behandlingen – vigtigheden af at kontrollere mindst årlige uACR og eGFR og dermed eskalering i håndteringen efter CKD-detektion ; (ii) integreret arbejdsgang, for eksempel forbedringer af elektroniske sygejournaler, for at inkludere registeroptimering for patienter med kronisk nyreinsufficiens, klinisk beslutningsstøtte eller andre opfordringer til at bestille de passende tests og udvalgte medicin, delte beslutningstagningsværktøjer og handlingsvenligt dashboard for befolkningen sundhedsforvaltning; og (iii) lukning af udestående henvisningssløjfer og plejehuller. En integreret sundhedssystem albuminuri CKD test kvalitetsinitiativ undersøgelse resulterede i en 56,1 procent stigning i opsamling af urin albumin i år et og en 50,1 procent stigning på 2 år; dog var der ingen korreleret statistisk forbedring i brugen af ACEi eller ARB hos disse patienter, hvilket muligvis indikerer en mulighed for evaluering af patientcyklus og forbedringer i uddannelse og operationsflow.
Et kvalitetsforbedringsprojekt, der implementerede primærplejebefolkningens sundhed for diabetes og hypertension med interventioner baseret på eGFR- og uACR-risikostratificeringen afslørede reduceret hospitalsindlæggelse, reduceret 30-dage-genindlæggelse og udvalgt lægemiddel pr. patient pr. måned omkostningsbegrænsning i et kommercielt sundhedsvæsen forsikringsplanens patientcentrerede medicinske boligmodel. Dette kvalitetsforbedringsprojekt er relativt lille og har mange begrænsninger, herunder minimal indvirkning på lav uACR-testning og manglende inkorporering af SGLT-2i i interventionen, men det er vigtigt, fordi resultaterne på kort sigt tyder på, at potentiel omkostningseffektivitet af CKD kvalitetsforbedring. Et imponerende langsigtet kvalitetsforbedringsinitiativ i det indiske sundhedsvæsen resulterede i en dramatisk reduktion på 54 procent af hændelse af ESKD for type 2-diabetes-populationen. Implementering af interventioner, der står i rimeligt forhold til spektret af CKD-risikostratificering ved eGFR og uACR, er et nøgleelement i kvalitetsforbedrende interventioner. Derudover er befolkningsafledte forudsigelsesmodeller såsom nyresvigtrisikoligningen og nye biomarkørpaneler integreret med den elektroniske patientjournal blevet brugt til at hjælpe med at vejlede henvisninger for at hjælpe med at informere primære klinikere om at udvælge patientpopulationen til at tilbyde tværfaglig behandling, såsom MNT og nefrologiske tjenester til patienter med den højeste risiko. Endelig tilbyder National Kidney Foundation kvalitetsforbedring CKD-ændringspakken en række værktøjer, der selektivt kan inkorporeres til det kliniske sted eller sundhedssystemets integration.
Betalingsmodeller
Chronic Care Model (CCM) er en effektiv tilgang til at organisere CKD-pleje med eksempler, herunder navigator-ledet, sygeplejerske-ledet, farmaceut-ledet, multidisciplinær specialist-ledet og patient-centreret. CCM-tilgange, hvor sundhedsprofessionelle leverer pleje i henhold til en struktureret protokol, kan forbedre overholdelse af behandlingsmål. Den navigator-ledede CCM for CKD G3b og G4 var mulig at implementere i 2 år, men den afslørede ikke forbedrede processer for laboratorietest og nefrologisk konsultation eller væsentligt forbedret eGFR-hældning. CCM-funktioner såsom registerfunktion, kliniske beslutningsstøtteinterventioner og tværfaglig pleje har vist sig at forbedre processer relateret til CKD-behandling, men med begrænset eller blandet effekt på patientresultater. CCM-design med betalingsmodeller afslørede CKD-resultater, herunder reduceret indlæggelse og reduceret dialysestart.
Centrene for Medicare og Medicaid Services implementerede 4 plejemodeller for CKD i januar 2022; Kidney Care First Option og 3 Comprehensive Kidney Care Contracting Graduated, Professional og Global Model Options tildeler ansvaret til en nefrologisk praksis eller en gruppe af sundhedspersonale for at tage sig af CKD G4 og G5 og dialyse med fokus på at forsinke CKD progression og håndtere overgangen til dialyse, øget nyretransplantation og støtte til sundhed efter nyretransplantation for at reducere omkostningerne og forbedre kvaliteten af plejen til patienter, hvilket yderligere vil informere omkostningseffektiviteten af CKD-betalingsmodeller. Selvom disse modeller er begrænset til nefrologisk pleje, er designet af Comprehensive Kidney Care Contracting baseret på Primary Care First og Global og Professional Direct Contracting-modellerne. Resultaterne kunne også tjene som grundlag for CKD-betalingsmodeller i primærpleje, koordineret med nefrologiske plejemodeller. Det kontraktlige forhold mellem Centers for Medicare og Medicaid Services med Medicare Advantage og dets indflydelse på kommercielle planer kan også udvide importen af resultaterne.

Cistanche piller
Resumé
En CKD-befolkningssundhedsstrategi (figur 2) bør bygges for at imødegå huller i primærpleje og implementering ud fra perspektiverne af test, påvisning af sygdom, interventioner og koordineret systemintegreret pleje. Registerfunktion og dataovervågning af CKD-byrden, leveringsinterventioner og resultater er nøglefunktioner. Implementering af de Race-free 2021 CKD-EPI eGFR-rapporteringsanbefalinger ved at engagere lokale nefrologiske, administrative, kliniske laboratorie- og sundhedsmæssige ledere bør hjælpe med at drive strategien og datavurderingen af befolkningens sundhedsdesign.

Referencer
1 Centre for Disease Control and Prevention. Overvågningssystem for kroniske nyresygdomme. Åbnet den 10. februar 2022.
2. United States Renal Data System. 2021 USRDS årlige datarapport. Epidemiologi af nyresygdomme i USA.: National Institutes of Health, National Institute of Diabetes and Digestive and Kidney Diseases: 2021.
3. National Kidney Foundation. K/DOQI retningslinjer for klinisk praksis for kronisk nyresygdom: evaluering, klassificering og stratificering. Am J Nyre Dis. 2002;39(suppl 2): S1– S266.
4. Nyresygdom: Forbedring af globale resultater (KDIGO) CKD-arbejdsgruppe. KDIGO 2012 kliniske retningslinjer for evaluering og behandling af kronisk nyresygdom. Nyre Int Suppl. 2013;3:1-150.
5. Inker LA, Astor BC, Fox CH, et al. KDOQI US-kommentar til 2012 KDIGO klinisk praksis retningslinjer for evaluering og håndtering af CKD. Am J Nyre Dis. 2014;63:713-735.
6. Tummalapalli SL, Powe NR, Keyhani S. Tendenser i kvaliteten af pleje for patienter med CKD i USA. Clin J Am Soc Nephrol. 2019;14:1142-1150.
7. Szczech LA, Stewart RC, Su HL, et al. Primærplejedetektion af kronisk nyresygdom hos voksne med type-2 diabetes: ADD-CKD-undersøgelsen (bevidsthed, påvisning og lægemiddelbehandling ved type 2-diabetes og kronisk nyresygdom). PLoS One. 2014, 26;9(11):e110535.
8. Delgado C, Baweja M, Burrows NR, et al. Revurdering af inklusion af race i diagnosticering af nyresygdomme: en foreløbig rapport fra NKF-ASN-taskforcen. Am J Nyre Dis. 2021;78:103-115.
9. Vyas DA, Eisenstein LG, Jones DS. Skjult i almindeligt syn - genovervejer brugen af racekorrektion i kliniske algoritmer. N Engl J Med. 2020;383:874-882.
10. Borrell LN, Elhawary JR, Fuentes-Afflick E, et al. Race og genetiske herkomst i medicin - en tid til opgør med racisme. N Engl J Med. 2021;384:474-480.
11. Diamantidis C, Cook D, Westman J, et al. Manglende pleje: virkningen af COVID-19-pandemien på CKD-pleje. Am J Nyre Dis. 2021. Udgivet online 2021.
12. American Diabetes Association Professional Practice B Draznin, VR Aroda. Kronisk nyresygdom og risikostyring: standarder for medicinsk behandling i diabetes-2022. Diabetes pleje. 2022;45(Supplement 1):S175–S184.
13. Tonelli M, Dickinson JA. Tidlig påvisning af CKD: konsekvenser for lande med lav indkomst, mellemindkomst og høj indkomst. J Am Soc Nephrol. 2020;31:1931-1940.
14. Shlipak MG, Tummalapalli SL, Boulware LE, et al. Sagen om tidlig identifikation og intervention af kronisk nyresygdom: konklusioner fra en nyresygdom: konference om forbedring af globale resultater (KDIGO). Nyre Int. 2021;99:34–47.
15. Stempneiwicz N, Vassalotti JA, Cuddeback JK, et al. Kronisk nyresygdomstest blandt primærplejepatienter med type 2-diabetes på tværs af 24 amerikanske sundhedsorganisationer. Diabetes pleje. 2021;44:2000–2009.
16. Alfego D, Ennis J, Gillespie B, et al. Testning af kroniske nyresygdomme blandt voksne i risikogruppen i USA er fortsat lav: beviser fra den virkelige verden fra en National Laboratory-database. Diabetes pleje. 2021;44:2025-2032.
17. Vassalotti JA, Argyropoulos C. Kan samfundsbaseret albuminuritestning forbedre plejen? Kidney Int Rep. 2020;5:392– 395.
18. Levey AS, Inker LA, Coresh J. "Skal definitionen af CKD ændres til at omfatte alderstilpassede GFR-kriterier?": Con: Evaluering og håndtering af CKD, ikke definitionen, bør alderstilpasses. Nyre Int. 2020;97:37–40.
19. Sumida K, Nadkarni GN, Grams ME, et al. Konvertering af urinprotein-kreatinin-forhold eller urinstiksprotein til urinalbumin-kreatinin-forhold til brug ved screening og prognose for kronisk nyresygdom: en individuel deltagerbaseret metaanalyse. Ann Intern Med. 2020;173:426-435.
20. Miller WG, Kaufman HW, Levey AS, et al. National Kidney Foundation Laboratory Engagement Working Groups anbefalinger til implementering af CKD-EPI 2021 race-fri ligninger for estimeret glomerulær filtrationshastighed: praktisk vejledning til kliniske laboratorier. Clin Chem. Udgivet online 16. december 2021
21. Inker LA, Eneanya ND, Coresh J, et al. Nye kreatinin- og cystatin C-baserede ligninger til at estimere GFR uden race. N Engl J Med. 2021;385:1737-1749.
22. Delgado C, Baweja M, Crews DC, et al. En samlende tilgang til GFR-estimering: anbefalinger fra NKF-ASN Task Force om revurdering af inklusion af race i diagnosticering af nyresygdom. Am J Nyre Dis. 2021;79:268-288.
23. Allen AS, Forman JP, Orav EJ, et al. Primær pleje af kronisk nyresygdom. J Gen Intern Med. 2011;26: 386-392.
24. Nyresygdom: Improving Global Outcomes (KDIGO) Diabetes Work Group. KDIGO 2020 kliniske retningslinjer for diabetesbehandling ved kronisk nyresygdom. Nyre Int. 2020;98:S1–S115.
25. Kramer HJ, Townsend RR, Griffin K, et al. KDOQI US kommentar til 2017 ACC/AHA hypertension guideline. Am J Nyre Dis. 2019;73:424-458.
26. Nyresygdom: Forbedring af globale resultater (KDIGO) Blood Pressure Work Group. KDIGO 2021 kliniske retningslinjer for håndtering af blodtryk ved kronisk nyresygdom. Nyre Int. 2021;99:S1-S87.
27. Bansal N, Zelnick L, Bhat Z, et al. Byrde og resultater af hjertesvigt indlæggelser hos voksne med kronisk nyresygdom. J Am Coll Cardiol. 2019;73:2691-2700.
28. Jankowski J, Floege J, Fliser D, et al. Kardiovaskulær sygdom i kronisk nyresygdom patofysiologisk indsigt og terapeutiske muligheder. Cirkulation. 2021;143:1157-1172.
29. Krueger KM, Ison MG, Ghossein C. Praktisk vejledning til vaccination i alle stadier af CKD, inklusive patienter behandlet med dialyse eller nyretransplantation. Am J Nyre Dis. 2020;75: 417-425.
30. Vassalotti JA, Centor R, Turner BJ, et al. National Kidney Foundation Kidney Disease Outcomes Quality Initiative. En praktisk tilgang til påvisning og behandling af kronisk nyresygdom for den primære læge. Am J Med. 2016;129:153– 162.e7.
31. Thavarajah S, Knicely DH, Choi MJ. CKD for primære praktiserende læger: kan vi skære ind i benet uden for mange genveje? Am J Nyre Dis. 2016;67:826-829.
32. Epping-Jordan JE, Pruitt SD, Bengoa R, Wagner EH. Forbedring af kvaliteten af sundhedspleje til kroniske lidelser. Qual Saf Health Care. 2004;13:299-305.
33. Nuño R, Coleman K, Bengoa R, Sauto R. Forbedring af kvaliteten af sundhedspleje til kroniske tilstande. Sundhedspolitik. 2012;105: 55-64.
34. Evans JM, Wheeler SM, Sati S, et al. Vurdering af levering af koordineret pleje til patienter med fremskreden kronisk nyresygdom i Ontario, Canada: en undersøgelse af patienter og sundhedspersonale. Int J Integr Care. 2021;21:30.
35. Kramer H, Jimenez EY, Brommage D, et al. Medicinsk ernæringsterapi til patienter med ikke-dialyseafhængig kronisk nyresygdom: barrierer og løsninger. J Acad Nutrit Diet. 2018;118:1958-1965.
36. Jimenez EY, Kelley K, Schofield M, et al. Adgang til medicinsk ernæringsterapi i CKD: en tværsnitsundersøgelse af patienter og udbydere. Nyre Med. 2020;3:31–41.e1.
37. Ikizler TA, Burrowes JD, Byham-Gray LD, et al. KDOQI klinisk praksis guideline for ernæring i CKD: 2020 opdatering [publiceret korrektion vises i Am J Kidney Dis. 2021;77:308]. Am J Nyre Dis. 2020;76(3 Suppl 1): S1–S107.
38. Greer RC, Liu Y, Cavanaugh K, et al. Primære lægers opfattede barrierer for nefrologisk henvisning og samtidig behandling af patienter med CKD: en kvalitativ undersøgelse. J Gen Intern Med. 2019;34:1228-1235.
39. Mendu ML, Waikar SS, Rao SK. Sundhedsstyring af nyresygdomme i en æra af ansvarlig pleje: en konceptuel ramme til optimering af pleje på tværs af CKD-spektret. Am J Nyre Dis. 2017;70:122-131.
40. Miller WG, Bachmann LM, Delanghe JR, et al. Optimal brug af biomarkører for kronisk nyresygdom. Clin Chem. 2019;65: 949-955.
41. American Society for Clinical Pathology. Tilgået 11. januar 2022.
42. National Kidney Foundation, Change Package CKD. Tilgået 11. januar 2022.
43. Den nationale komité for kvalitetssikring, HEDISR tekniske specifikationer, bind 2, 2022.
44. Mendu ML, Tummalapalli SL, Lentine KL, et al. Måling af kvalitet i nyrepleje: en evaluering af eksisterende kvalitetsmålinger og tilgang til at lette forbedringer i plejelevering. J Am Soc Nephrol. 2020;31:602-614.
45. Park KJ, Unitan RS, Thorp ML. Et kvalitetsforbedringsinitiativ rettet mod mål for kroniske nyresygdomme gennem øget albumintestning i urinen. Per M J. 2020;25:1.
46. Vassalotti JA, DeVinney R, Lukasik S, et al. CKD kvalitetsforbedringsintervention med PCMH-integration: sundhedsplanresultater. Am J Manag Care. 2019;25:e326–e333.
47. Narva A. Befolkningssundhed for CKD og diabetes: lektioner fra det indiske sundhedsvæsen. Am J Nyre Dis. 2018;71: 407-411.
48. Tangri N, Grams ME, Levey AS, et al. Multinational vurdering af nøjagtigheden af ligninger til forudsigelse af nyresvigt: en meta-analyse [publiceret korrektion vises i JAMA. 2016;315:822]. JAMA. 2016;315:164-174.
49. Nicoll R, Robertson L, Gemmell E, et al. Modeller for pleje af kronisk nyresygdom: en systematisk gennemgang. Nephrol (Carlton). 2018;23:389-396.
50. Navaneethan SD, Jolly SE, Schold JC, et al. Pragmatisk randomiseret, kontrolleret undersøgelse af patientnavigatorer og forbedrede personlige helbredsjournaler i CKD. Clin J Am Soc Nephrol. 2017;12:1418-1427.
51. Centre for Medicare og Medicaid Services. Tilgået 11. januar 2022.
Joseph A. Vassalotti 1,2 og Suelyn C. Boucree 3.
1 afdeling for nefrologi, afdeling for medicin, Icahn School of Medicine ved Mount Sinai, New York, New York, USA;
2 Det National Nyre Foundation, Inc., Ny York, Ny York, USA;
3 Hackensack Meridian Health Network, Hackensack, New Jersey, USA.
