En sletning af fem aminosyrer i NKCC2 af C57BL/6-mus påvirker analyse af NKCC2-phosphorylering, men påvirker ikke nyrefunktionen
Feb 19, 2022
INTRODUKTION
Pattedyrets tykke opstigende lem (TAL).nyreer afgørende for kontrollen af ekstracellulær væskevolumen, urinkoncentration, calcium (Ca 2 plus ) og magnesium (Mg 2 plus ) homeostase, samt pH-balance. 1 Den vigtigste Na plus transportvej i TAL er Na plus - K plus - 2Cl − cotransporteren (NKCC2), som er specifikt hæmmet af loop-diuretika. 1 Cotransporten af Na plus, K plus og 2Cl − ioner via NKCC2 er elektroneutral, men afhænger af elektrogen K plus sekretion via apikalen nyreydre medulla K plus kanal ROMK. 2 Samspillet mellem NKCC2 og ROMK skaber en lumen-positiv elektrokemisk gradient, der forbedrer Na plus reabsorption og driver den paracellulære transport af Ca 2 plus og Mg 2 plus . 3 Betydningen af NKCC2 for TAL ognyrefunktioner eksemplificeret ved Bartter type I syndrom, en genetisk lidelse forårsaget af funktionstab mutationer i NKCC2, der viser sig med alvorligenyresalt- og væskespild, hypokalæmisk metabolisk alkalose og hypercalciuri. 3
NKCC2 er medlem af den opløste bærerfamilie 12 (Slc12) af membrantransportproteiner, der også inkluderer den allestedsnærværende udtrykte NKCC1 og den distale indviklede tubulus (DCT) specifikke Na plus - Cl - cotransporter (NCC). 2 Aktiviteten af NKCC2 korrelerer positivt med phosphorylering af cotransporteren ved adskillige serin- og threoninrester på den cytoplasmatiske N-terminale hale. 4 Aminosyresekvenserne omkring disse phosphoryleringssteder er meget konserverede og viser en høj grad af lighed blandt NKCC2, NKCC1 og NCC. 2 Fosforyleringen af NKCC2 stimuleres af flere hormonelle og ikke-hormonelle veje. Hormoner såsom arginin vasopressin (AVP) og angiotensin II (ANGII) stimulerer NKCC2 via øget cAMP-produktion og aktivering af proteinkinase A (PKA). 5 PKA menes at phosphorylere NKCC2 direkte ved Ser126, hvilket øger exocytosen af NKCC2-holdige vesikler og dermed overfloden af transportøren i den apikale plasmamembran. 6 Ligeledes regulerer ændringer i intracellulære chloridkoncentrationer NKCC2-phosphorylering. En sænket tracellulær Cl − koncentration stimulerer uden-lysin(K) kinaserne WNK1 og WNK4 til at phosphorylere og aktivere de nedstrøms kinaser Ste20- relaterede prolin alanin rig kinase (SPAK) eller oxidativ stress responsive kinase 1 (OXSR1) ). 7- 9 Efter binding til et "RFxV"-motiv i NKCC2, phosphorylerer disse kinaser derefter NKCC2 ved to threoninrester (T96 og T101). 2 Dephosphorylering af disse rester medieres af phosphatasen calcineurin, hvilket understreger, at NKCC2 er et mål for flere signalveje. 10

For at studere NKCC2-funktionen udviklede flere grupper, inklusive vores, phosphoform-specifikke antistoffer mod Thr96 og/eller Thr101. 11- 17 Antistofferne blev brugt til at vurdere NKCC2-phosphorylering i heterologe ekspressionssystemer 7,11,17,18,19,20 og dyremodeller inklusive rotter 10,21,22,23,24,25 og mus. 14,15,16,17,19,26,27 Men når vi brugte vores pT96/101 NKCC2 antistof, opnåede vi inkonsistente resultater i vores forskellige musemodeller. Mens vi detekterede stærke pNKCC2-signaler i nyrer fra mus i en 129Sv genetisk baggrund, fik vi ikke pålidelige pNKCC2-signaler i nyrer fra C57BL/6-mus, men observerede en krydsreaktivitet af pNKCC2-antistofferne med pNCC. Andre laboratorier, inklusive dem fra JA McCormick og AA McDonough (personlig kommunikation) gjorde lignende observationer. 18,28,29 Desuden er slående stammeforskelle blevet beskrevet hos mus fornyrefunktion 30 inklusive signifikant lavere urin Ca 2 plus udskillelse i C57BL/6 sammenlignet med 129Sv mus. 31 Derfor antog vi, at C57BL/6-mus udtrykker en genetisk variant af NKCC2, der påvirker NKCC2-phosphorylering og evt.nyrefunktionder forklarer de observerede belastningsforskelle. Den følgende undersøgelse var designet til systematisk at teste denne hypotese.
Nøgleord:ionhomeostase, nyre, NKCC2, phosphorylering, stammeforskelle
RESULTATER
2.1|C57BL/6-mus har en deletion af fem aminosyrer i NKCC2, der interfererer med påvisningen af phosphoryleret NKCC2Først justerede vi for flere arter de publicerede N-terminale aminosyresekvenser (transkriptions-ID'er i tabel S1) af NKCC2 og NCC (henholdsvis figur 1A, B), der svarer til epitoperne genkendt af anti-pNCC og anti-pNKCC antistofferne (Figur 1C). Justeringen bekræftede den høje grad af konservering af phosphoryleringsstederne for NKCC2 og NCC 7, der sandsynligvis forklarer krydsreaktiviteten af pNKCC2- og pNCC-antistofferne observeret af os og andre. 18,28,29 Interessant og i overensstemmelse med vores hypotese afslørede justeringen også en hidtil ikke værdsat deletion af fem aminosyrer i sekvensen af NKCC2 fra C57BL/6 mus (ΔF97- T101) (Figur 1A) . Sekventering af DNA'et fra to forskellige C57BL/6 musekolonier holdt på The Jackson Laboratory i USA eller Janvier Labs i Frankrig bekræftede en nukleotiddeletion i exon 2 af C57BL/6 NKCC2, der svarer til ovennævnte aminosyredeletion (figur S1) Tabel S2).
For at karakterisere virkningen af deletionen af fem aminosyrer på immundetekteringen af total og fosforyleret NKCC2, undersøgte vi systematisk nyrer fra C57BL/6 og 129Sv mus ved immunhistokemi og immunoblotting. Immunfluorescens med et antistof mod total NKCC2 viste et stærkt fluorescerende signal i den apikale plasmamembran af TAL'er fra 129Sv og C57BL/6 mus. Vores tidligere udviklede pT96/T101 NKCC2-antistof viste imidlertid en stærk apikal mærkning af TAL'er kun i 129Sv-mus, mens TAL'er af C57BL/6-mus havde en meget svag immunfarvning (figur 1D). I overensstemmelse med dette afslørede Western blot-analyse et stærkt bånd for total NKCC2 i begge musestammer, mens pT96/T101 NKCC2-antistoffet kun påviste et stærkt bånd ved den forventede størrelse (170 kDa) i 129Sv-mus (figur 1E). I stedet afslørede nyrer af C57BL/6 mus et bånd ved 130 kDa, der svarer til den forventede størrelse af NCC (figur 1E). Lignende resultater blev opnået med andre antistoffer, der tidligere blev brugt til at studere NKCC2-phosphorylering (figur S2). pT212/T217 NKCC1 R5-antistoffet 11 viste ud over pNCC-signalet et svagt signal ved den forventede størrelse for pNKCC2 (figur S2). Det immunreaktive bånd for pNKCC2 blev mere intenst, når det var frisknyrelysater blev brugt. Brugen af en lyseringsbuffer med detergenter (RIPA-buffer) forbedrede ikke, men formindskede signalintensiteten (figur S3).
FIGUR 1 pT96/T101 NKCC2-antistoffet detekterer ikke et synligt pNKCC2-signal i C57BL/6-mus. A, NKCC2-aminosyresekvensjustering af forskellige arter og de to musestammer 129Sv og C57BL/6. NKCC2-sekvens-ID'erne for de forskellige arter er opført i tabel S1. Den meget konserverede region svarende til murint Thr96 til murint Thr101 er markeret med gråt. B, Aminosyresekvensjustering af NCC i forskellige arter. NCC-sekvens-ID'erne for de forskellige arter er opført i tabel S1. C, Liste over epitoper af almindeligt anvendte og publicerede antistoffer, der genkender pT53 eller pT58NCC, såvel som pNKCC2 ved det konserverede locus omkring Thr96 til Thr101. D, Immunfarvning af total og pT96/T101 NKCC2 i konsekutive kryosnit af mus med 129Sv og C57BL/6 baggrund. Målestok=50 µm. E, Immunoblot af total og pT96/T101 NKCC2 fra mus med 129Sv og C57BL/6 baggrund. Værdier er middelværdier ± SEM, n=5 mus pr. gruppe, de grønne pile peger på de specifikke bånd, mens de røde pilehoveder peger på de ikke-specifikke bånd. Molekylvægtsmarkører er inkluderet. Total- og pT96/T101 NKCC2-bånd forventes at være på 170 kDa. F, Immunoblots for total og pT96/T101 NKCC2, total og pT53 og pT58 NCC i NCC WT og NCC knockout (KO) mus med forskellig baggrund. De grønne pile peger på de specifikke bånd, mens de røde pilehoveder peger på de ikke-specifikke bånd. Molekylvægtsmarkører er inkluderet. Total og pT58 og pT53 NCC bånd forventes ved 130 kDa, totale og pT96/T101 NKCC2 bånd forventes ved 170 kDa
For at teste, om vores pT96/T101 NKCC2-antistof faktisk krydsreagerer med phosphoryleret NCC i C57BL/6-mus, undersøgte vinyrelysater fra 129Sv og C57BL/6 vildtype mus og C57BL/6 NCC knockout mus med antistoffer mod total NKCC2, pT96/T101 NKCC2, total NCC og phosphoryleret NCC (pT53 og pT58 NCC) (figur 1F). pT96/T101 NKCC2-antistoffet og antistoffer mod total NCC og pNCC detekterede ikke bånd ved 130- 170 kDa i C57BL/6 NCC-knockout-musene (figur 1F). Interessant nok indikerer immunblotten såvel som yderligere immunhistokemiske eksperimenter (figur S4), at ikke kun pNKCC2-antistofferne krydsreagerer med NCC i C57BL/6-mus, men vores pNCC-antistoffer (pT53 NCC og pT58 NCC) krydsreagerer med NKCC2 i 129Sv mus i de anvendte koncentrationer.
Udskillelse af calcium og magnesium i urinen er forskellig mellem 129Sv og C57BL/6 mus
For at bestemme, om deletionen (F97- T101) i NKCC2 kan associere med fysiologiske forskelle mellem 129Sv og C57BL/6 mus, sammenlignede vi vandindtag, plasmaionniveauer og urinvæske og ionudskillelse mellem de to musestammer. Som opsummeret i tabel 1 var de fleste af de vurderede parametre ikke forskellige mellem stammerne. C57BL/6 mus viste imidlertid en lavere urin Ca 2 plus og højere urin Mg 2 plus udskillelse end 129Sv mus. Plasma Ca 2 plus og Mg 2 plus niveauerne var ens for begge grupper, hvilket tyder på, at musene var i en steady-state, hvor en homøostatisk balance mellem intestinal reabsorption, vævsmobilisering (f.eks. fra knogler) ognyreudskillelse af Ca 2 plus og Mg 2 plus ioner blev nået. For at teste, om de forskellige urinudskillelseshastigheder for Ca 2 plus og Mg 2 plus skyldes forskelle i tarmens optagelse af disse ioner, sammenlignede vi daglig fødeindtagelse, fækal produktion og fækal Ca 2 plus og Mg 2 plus udskillelse for de to musestammer. Som vist i figur S5 var fødeindtagelse og fækal Ca 2 plus udtag ens, men den daglige fæces Mg 2 plus udskillelse var lavere i C57BL/6 mus end i 129Sv mus, hvilket tyder på, at C57BL/6 mus har højere intestinal Mg 2 plus reabsorption end 129Sv mus. I overensstemmelse med denne antagelse havde C57BL/6-mus stærkere tyktarmsekspression af magnesiumkanalen TRPM6 (figur S6) såvel som en tendens til højere plasma Mg 2 plus-niveauer sammenlignet med 129Sv-mus, selvom forskellene ikke nåede statistisk signifikans. For at vurdere knoglens mulige bidrag analyserede vi ved mikro-CT knoglemineraltætheden i begge stammer. I lighed med tidligere rapporter havde 32 C57BL/6-mus en ret lav knoglemineraltæthed (figur S7), hvilket kan forklare, hvorfor disse mus har tendens til at bevare Ca 2 plus-ioner via en reduceretnyreCa 2 plus udskillelse. I overensstemmelse med en forbedret tubulær Ca 2 plus reabsorptionshastighed, nyrerne af C57BL/6 mus
udtrykte mere TRPV5 Ca2 plus-kanal ved proteinniveauer end nyrer fra 129Sv mus (figur 2). C57BL/6-mus havde også en signifikant større NCC-mRNA og proteinekspression end 129Sv-mus (figur 2A). På samme måde var proteinoverfloden af total NKCC2, total og phosphoryleret NCC og af total - ENaC højere i C57BL/6 end i 129Sv mus (figur 2B,C). Overflod af de proteolytisk spaltede og dermed aktive former af - og - ENaC var ikke forskellige, hvilket tyder på, atnyreENaC-aktivitet var ens for begge stammer (figur 2B, C).
Ingen evidens for en ændret funktion af tykt stigende lem hos C57BL/6-mus sammenlignet med 129Sv-mus
De højere forekomster af total NKCC2, total NCC og phosphoryleret NCC i nyrer fra C57BL/6-mus kan være en kompenserende respons for reduceret NKCC2-phosphorylering. For at teste, om aktiviteten af NKCC2 og NCC adskiller sig mellem musestammerne, udførte vi henholdsvis en bumetanid- og thiazid-test. En enkelt injektion af bumetanid eller hydrochlorthiazid fremkaldte en stærk natriurese, som var mere udtalt for bumetanid end for hydrochlorthiazid. Imidlertid var de diuretiske reaktioner fuldstændig ens i begge stammer, hvilket tyder på, at de funktionelle aktiviteter af NKCC2 og NCC ikke var forskellige mellem C57BL/6 og 129Sv mus (figur 3A-D). Tilsyneladende passer proteinoverflod og fosforyleringsniveauer ikke nødvendigvis sammen med de funktionelle aktiviteter afnyreiontransportproteiner som for nylig også påpeget af Hunter og kolleger. 33 For yderligere at vurdere TAL-funktionen udførte vi en vandrestriktionstest, hvor mus i 24 timer havde adgang til fugtet foder, men ikke til postevand. Under disse betingelser øgede begge musestammer urinosmolariteten til lignende værdier (tabel 1). Endvidere viste C57BL/6 mus og 129Sv mus den samme urinudskillelse af uromodulin (Tamm-Horsfall protein) (tabel 1), som produceres og udskilles i urinen afhængigt af TAL-cellernes funktionelle aktivitet. 3

Krydsning af 129Sv og C57BL/6 mus tyder på, at deletionen af fem aminosyrer i NKCC2 ikke adskiller en specifik fænotype
De præsenterede data tyder på, at stammeforskellene i urin-ionudskillelse ognyreproteinoverflod er ikke relateret til de fem aminosyredeletioner i C57BL/6 NKCC2, men er relateret til andre genetiske forskelle mellem de to musestammer. For at teste dette yderligere, krydsede vi 129Sv- og C57BL/6-mus til F2-generationen, hvor genetiske stammeforskelle (inklusive dem i NKCC2) skulle være tilfældigt

fordelt til musene. Vi sammenlignede derefter F2-mus, der enten var homozygote for fuldlængde NKCC2 (f/f), homozygote for NKCC2-deletionen (Δ/Δ) eller heterozygote for NKCC2-deletionen (f/Δ). Med undtagelse af de forventede forskellige bindingsmønstre af de phosphoform-specifikke antistoffer mod NKCC2 og NCC (og en uklar forskel i ROMK-ekspression på mRNA-, men ikke proteinniveau), var ingen af de tidligere identificerede forskelle mellem de to stammer tydelige i f/f-, Δ/Δ- eller f/Δ-musene af F2-generationen (figur 4 og tabel 2). Især var der ingen forskelle i den urinære Ca 2 plus eller Mg 2 plus udskillelse, samt ingen forskelle i plasma Ca 2 plus eller Mg 2 plus niveauer, hvilket tyder på, at stammeforskellene mellem 129Sv og C57BL/6 mus er uafhængige af de fem aminosyrer deletion i NKCC2.
Et nyt pT96 NKCC2-antistof detekterer pNKCC2 i begge stammer
Da deletionen af fem aminosyrer i NKCC2 hindrer en pålidelig påvisning af NKCC2-phosphorylering i C57BL/6-mus ved brug af tilgængelige antistoffer, genererede vi et nyt antistof rettet mod T96-phosphositet i C57BL/6-mus. Kaniner blev immuniseret med et phosphopeptid, der svarede til aminosyresekvensen af C57BL/6 NKCC2, der omgiver T96 (YYLQ(p)TMDA). Antisera blev affinitetsoprenset og karakteriseret ved immunoblotting og immunhistokemi (figur 5). Antistoffet detekterede et enkelt bånd ved den forventede størrelse på 170 kDa i nyrer af 129Sv, C57BL/6 vildtype og C57BL/6 NCC knock-out

mus (figur 5A). Båndet var klart forskelligt fra det, der blev detekteret for NCC ved 130 kDa. Dephosphorylering af 129Svnyreprøver med kalvetarm-alkalisk fosfatase (CIAP) udryddede fuldstændigt signalet opnået med det nye pT96 NKCC2-antistof, mens signalet med det ikke-phosphoform-specifikke NKCC2-antistof var synligt i kontrol- og dephosphorylerede prøver (figur 5B). Interessant nok blev NKCC2-phosphorylering også stort set elimineret nårnyrelysater blev inkuberet ved 37 grader i 1 time uden CIAP (sandsynligvis på grund af aktiviteten af endogen alkalisk phosphatase fra de proksimale tubuli). Dephosphoryleringseksperimenter under anvendelse af lambda-phosphatase på på hinanden følgende paraffin-nyresektioner af C57BL/6-mus bekræftede yderligere, at det nye antistof kun genkender phosphoryleret NKCC2 (figur 5C). Ydermere viste immunfluorescens på konsekutive kryosnit, at nye antistoffet kun farver den apikale plasmamembran af NKCC2- positive TAL'er, men ikke af NCC-positive DCT'er i 129Sv og C57BL/6 mus (figur 5D), hvilket tyder på, at den nye pNKCC2-antistof krydsreagerer ikke med pNCC. Denne konklusion blev også bekræftet under anvendelse af cellelysater fra MDCKI-celler, der udtrykker human NKCC2 (hNKCC2) og human NCC (hNCC). Immunoblots af immunpræcipitationer (IP) og helcellelysater viste, at det nye pT96 NKCC2-antistof genkender humant NKCC2, men ikke humant NCC (figur S8A). Interessant nok, selvom det nye antistof blev rejst mod pNKCC2 fra C57BL/6-mus, detekterede det nye antistof NKCC2-phosphorylering ækvivalent i nyrer fra begge musestammer ved både immunhistokemi (figur 6A) og immunoblotting (figur 6B).
Det nye pT96 NKCC2-antistof tillader analyse af reguleret NKCC2-phosphorylering
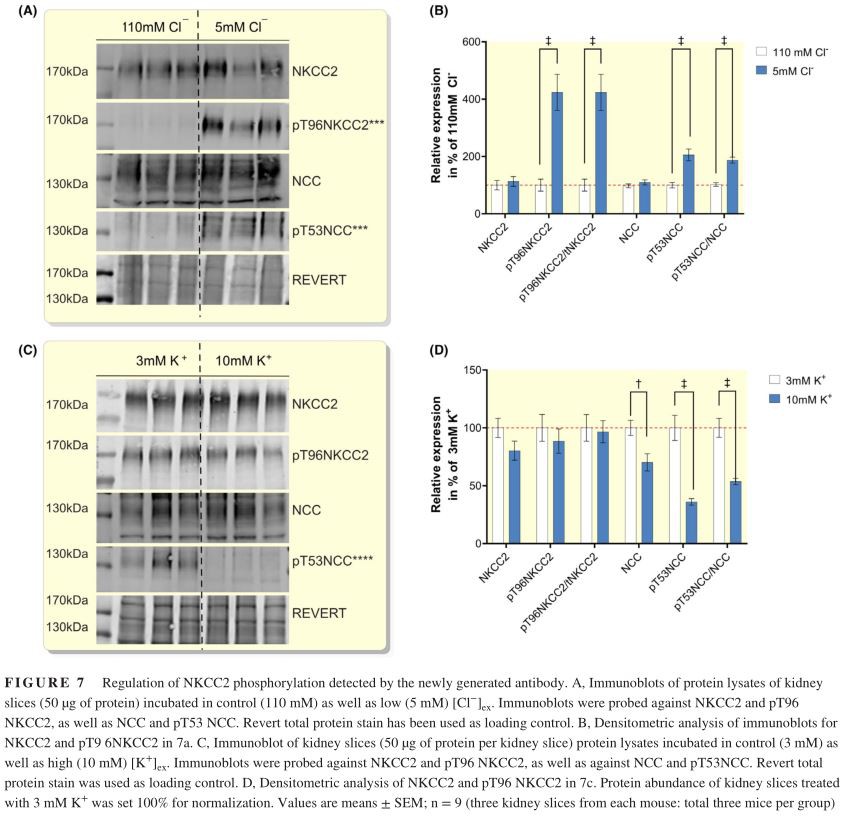
Fosforyleringen og dermed aktiviteten af NKCC2 og NCC reguleres af ekstracellulære ionkoncentrationer. En lav [Cl-] ex øger phosphoryleringen af NKCC2 ved Thr96 og Thr101 og af NCC ved Thr53 og Thr58 via aktivering af WNK/SPAK/OSR1-vejen. 7,8,18,29,35 Ligeledes nedsætter et højt [K plus ] hurtigt phosphoryleringen af NCC, men menes at have ringe eller ingen effekt på NKCC2-phosphorylering. 12,36,37,38 For at teste, om det nyudviklede pT96 NKCC2-antistof er i stand til at påvise denne type differentiel regulering af NKCC2-phosphorylering,nyreskiver af C57BL/6-mus blev eksponeret ex vivo for henholdsvis 110 eller 5 mM [Cl-] ex og til 3 eller 10 mM [K plus] ex. Som forventet øgede den lave [Cl-] ex kraftigt NCC og NKCC2 fosforylering (Figur 7A,B), mens den høje [K plus] ex kun reducerede NCC fosforylering, men ikke ændrede NKCC2 fosforylering (Figur 7C,D). Ligeledes var det nye antistof detekteret lige så godt ændret

FIGUR 4 Ingen signifikante ændringer i mRNA og proteinekspression af majornyreiontransportører og kanaler i den krydsede F2-generation. A, søjleplot af relative mRNA-ekspressionsniveauer i de tre grupper af mus. Alle værdier blev normaliseret til f/f-mus. Værdier er middelværdier ± SEM. B, Proteinoverflod i musnyrelysater fra dyr af F2-generationen. De tre grupper svarer til NKCC2 i fuld længde (f/f), NKCC2 homozygot for deletionen (Δ/Δ) eller NKCC2 heterozygot for deletionen (f/Δ/). Molekylvægtsmarkører er inkluderet. NKCC2 og pNKCC2 forventes ved 170 kDa, NCC og pNCC ved 130 kDa, TRPM6 ved 260 kDa, - ENaC ved 95 kDa og 34 kDa (spaltet), - ENaC ved 100 kDa, - ENaC ved 100 kDa og (clevet) ROMK ved 55 kDa (moden glycosyleret), 43 kDa (kerne glycosyleret) og 34 kDa (uglycosyleret). Grønne pile peger på de specifikke bånd, mens de røde pilehoveder peger på de ikke-specifikke bånd. C, Densitometrisk analyse af proteinoverflod ved sammenligning af f/f og Δ/Δ mus. Båndintensiteterne fra Δ/Δ-mus er normaliseret til dem fra f/f. (Værdier er middelværdier ± SEM; n=5 mus/gruppe; *P < 0,05,="" †="" p="">< 0,01,="" ‡="" p=""><>
NKCC2-phosphorylering, der blev fremkaldt i MDCKI-celler, der udtrykker human NKCC2 (hNKCC2) eller muse-NKCC2 (mNKCC2(C57BL/6)) ved hypotoniske lave ekstracellulære chloridforhold (figur S8B). Inyreskiver inkuberet ved 5 mM [Cl − ] ex, også de tidligere beskrevne anti-mus pT96/T101 NKCC2 39 og anti-humane pT212/T217 NKCC1 R5 11 antistoffer detekterer svage signaler for NKCC2 og NCC, som bliver mere indlysende, når flere proteiner er indlæst, og immunoblots afbildes ved forbedrede indstillinger (Figur S9).
DISKUSSION
C57BL/6 og 129Sv mus er to af de mest almindeligt anvendte musestammer til biomedicinsk forskning. Genomet af C57BL/6 mus var det første, der blev sekventeret for musen 40 og har siden fungeret som referencegenom til analyse af genetiske og fænotypiske variationer mellem musestammer. 41- 44 Fornyreforskning, en væsentlig forskel mellem C57BL/6 og 129Sv mus vedrører ekspressionen af reningenet. Ligesom mennesker har C57BL/6-mus kun ét reningen, mens 129Sv-musene har to kopier, hvilket kan forklare denne musestammes højere modtagelighed for hypertension 45,46 og hypertensive skader. 47 Med denne undersøgelse tilføjer vi endnu en vigtig genetisk forskel, som skal overvejes. Vi beskriver en hidtil ukendt deletion af fem aminosyrer i NKCC2 (ΔF97- T101), til stede i C57BL/6, men ikke i 129Sv-mus, som interfererer med påvisningen af NKCC2-phosphorylering med de fleste tidligere tilgængelige antistoffer, men som ikke er signifikant indvirkningnyrefunktion.
Muse NKCC2 N-terminale phosphoryleringssteder T96 og T101 er stærkt konserverede på tværs af arter og mellem NKCC2, NKCC1 og NCC (figur 1). 48 Derfor er det ikke overraskende, at antistoffer rettet mod disse phosphoryleringssteder krydsreagerer med de andre cotransportere. Tidligere undersøgelser har rapporteret, at antistoffer mod phosphoryleret NCC også detekterer phosphoryleret NKCC2 7,18,28,29, og at et pNKCC1-antistof tillader analyse af phosphoryleringsniveauerne af både NKCC1 og NKCC2. 11 I overensstemmelse med dette observerede vi krydsreaktivitet af vores pNCC (pT53 og pT58) antistoffer med phosphoryleret NKCC2 og af vores pT96/pT101 NKCC2 antistof med phosphoryleret NCC. Krydsreaktiviteten af pNCC-antistofferne med NKCC2 blev imidlertid kun set i nyrer fra 129Sv-mus, men ikke i nyrer fra C57BL/6-mus. Omvendt viste vores tidligere udviklede antistof mod NKCC2 pT96/pT101 intet eller i bedste fald et meget svagt signal for pNKCC2 i nyrerne på C57BL/6 mus og detekterede hovedsageligt phosphoryleret NCC i denne stamme. Nu forbinder vi disse forvirrende observationer til en sletning af fem aminosyrer i NKCC2 af C57BL6-mus (ΔF97- T101). Reguleringen af NKCC2-phosphorylering er blevet undersøgt
brugt i forskellige eksperimentelle omgivelser og til forskellige stimuli, herunder vasopressin, 14,21,24,25,49 uromodulin 19,20,50 og calcineurinhæmmere. 10,26 Mens de fleste af undersøgelserne blev udført i heterologe ekspressionssystemer 10,19,20,25,50 eller i rotter 10,24 og mus 19,26, der udtrykker NKCC2 i fuld længde, blev nogle undersøgelser også udført i C57BL/6-mus. 7,18,27,28,29,51 Som vi rapporterer her, udtrykker C57BL/6-mus en NKCC2-variant med en deletion på fem aminosyrer, der interfererer med den korrekte påvisning af NKCC2-phosphorylering, og som bærer risikoen for, at standard pT96/T101 NKCC2 antistoffer og R5 anti phospho-NKCC1 antistoffet krydsreagerer med phosphoryleret NCC i det mindste under de betingelser, der anvendes i vores arbejde. Det er ikke muligt at bedømme virkningen af denne krydsreaktion på tidligere eksperimentelle konklusioner, men ifølge vores observationer bør data fra C57BL/6-mus genbesøges og fortolkes med forsigtighed. På trods af det faktum, at deletionen af fem aminosyrer havde en stærk indflydelse på påvisningen af NKCC2-phosphorylering, har vi ingen beviser for, at deletionen signifikant påvirker cotransportørens funktionelle aktivitet. C57BL/6 mus havde faktisk en højere urin Mg 2 plus udskillelse og lavere urin Ca 2 plus udskillelse 31 end 129Sv mus, men vi fandt, at disse forskelle sandsynligvis ikke er relateret til en ændret paracellulær transport af disse kationer langs TAL, men er resultatet af en øget TRPM6- afhængig Mg 2 plus optagelse i tarmen og en øget TRPV5- afhængig Ca 2 plus reabsorption i DCT2 og CNT. Sidstnævnte forårsager en positiv Ca 2 plus balance, der kan hjælpe med at øge den lave knoglemineraltæthed af C57BL/6 mus. Konstateringen af, at C57BL/6 og 129Sv mus viser det sammenyrereaktioner på loop- og thiaziddiuretika og på vandrestriktion tyder yderligere på, at de fem aminosyrer deletion i NKCC2 ikke signifikant forringer TAL-funktionen. Vigtigst er det, at mus af F2-generationen af krydsavlede C57BL/6- og 129Sv-mus har det sammenyrefænotype uafhængig af om mus udtrykker fuld længde (f/f) NKCC2 eller NKCC2

homozygot (Δ/Δ) for deletionen. Disse observationer i mus er i overensstemmelse med tidligere funktionelle data fra heterologe ekspressionssystemer. Mens mutationer af enkelte rester i NKCC1 (T217 hos mennesker, T211 hos mus) eller NCC (T60 hos mennesker, T58 hos mus) ophæver aktiviteten af disse cotrans portører, mutationer af den tilsvarende rest i NKCC2 (T105 hos mennesker, T101 hos mus) ) har ret lille eller endda ingen effekt på baseline og stimuleret NKCC2-aktivitet. 35,52,53 Selv når begge threoninrester i NKCC2 er muteret til alanin, når den funktionelle aktivitet af NKCC2 stadig ~70 procent af maksimal aktivitet, 35 hvilket tyder på, at phosphoryleringen af disse steder er vejledende, men ikke afgørende for NKCC2-aktivitet.
Fosforyleringssteder er ofte homologe mellem proteiner. Derfor er problemet med krydsreaktivitet af phosphoform-specifikke antistoffer ikke unikt for antistoffer rettet mod phosphoryleret NCC, NKCC2 og NKCC1, men blev også rapporteret for andre proteiner såsom de cyclinafhængige kinaser 1 og 2 54 og den ekstracellulære signalregulerede kinaser 1 og 2. 55 Konsekvent, når der anvendes phosphoryleringstilstandsspecifikke antistoffer, er strenge eksperimentelle kontroller nødvendige for at bekræfte specificiteten af de detekterede signaler. Dette kan omfatte (a) bekræftelse af, at det anvendte antistof detekterer proteinet ved den forventede molekylvægt (immunoblotting) og/eller ved den forventede cellulære og subcellulære lokalisering (immunofluorescens), (b) verifikation af, at antistoffet interagerer specifikt med den phosphorylerede epitop vha. anvendelse af konkurrenceassays med de phosphorylerede og ikke-phosphorylerede peptider, og (c) demonstration af, at

antistoffet er phosphoform-specifikt ved at sammenligne phosphorylerede og dephosphorylerede vævsprøver. Disse kontroller kan suppleres med genetiske kontroller, der inkluderer testning af væv fra knockout-dyr og/eller celler, der heterologt udtrykker proteinet af interesse. I denne undersøgelse brugte vi ovennævnte tilgange til grundigt at karakterisere et nyt pT96 NKCC2-antistof, der detekterer phosphoryleret NKCC2 inyreprøver fra C57BL/6 og 129Sv mus lige godt. Antistoffet er phosphoform-specifikt og viser ingen tilsyneladende krydsreaktivitet med phosphoryleret NCC under nogen af de testede betingelser. Ved at bruge dette antistof bekræftede vi, at lave ekstracellulære chloridkoncentrationer øger phosphoryleringen af NKCC2 på dette sted, 7,8, mens ændrede ekstracellulære kaliumkoncentrationer ikke har en signifikant regulerende rolle. 24 Som konklusion afslører vores arbejde en kritisk stammeforskel i aminosyresekvensen af mus NKCC2, som påvirker påvisningen og dermed analysen af NKCC2-phosphorylering og -regulering. Et nyudviklet pT96 NKCC2-antistof omgår denne tekniske advarsel og tillader en pålidelig påvisning af ændret NKCC2-phosphorylering uafhængigt af den genetiske baggrund af musemodeller. Desuden understreger vores undersøgelse igen, at genetiske baggrundsforskelle skal tages i betragtning, når man analyserer musemodeller.
MATERIALER OG METODER
dyr,Han-aldersmatchede (6- 8 uger) mus var enten af indavlede stammer 129S6/SvEvTac, C57BL/6J, herved omtalt som 129Sv og C57BL/6, eller en blandet hybridstamme 129S/B6 i F2-generation. Alle dyreforsøg blev udført i overensstemmelse med schweizisk dyrevelfærdslovgivning og godkendt af veterinæradministrationen i kantonen Zürich, Schweiz (licenser: 141/2014, 185/2017 og 135/2018). Mus blev genotypebestemt til deletion af 15 baser ved hjælp af standard PCR med primere angivet i tabel S3. Fuldlængde (f/f) NKCC2 har et forventet PCR-produkt på 87 bp, mens deleteret NKCC2-sekvens (Δ/Δ) forventes ved 70 bp.
VævsbehandlingMus blev bedøvet med en kombination af isofluran (2 procent - 4 procent, 0,5 l/min; Provet; CH) og Temgesic (Buprenorphine; 0.05- 0. 4 mg/kg kropsvægt; Indivor; CH). Til biokemisk analyse blev mus bedøvet og perfunderet via hjertets venstre ventrikel med fosfatbufret saltvand (PBS). Nyrer og distale koloner blev høstet, lynfrosset i flydende nitrogen og opbevaret i -80 grader indtil videre behandling. Til immunhistokemi blev nyrerne fikseret ved hjælp af paraformaldehyd (PFA) 3 procent i 0,1 M fosfatbuffer (pH 7,4, 300 mOsm) ved retrograd perfusion af den dybt bedøvede mus via abdominalaorta efterfulgt af en kort skylning med 0,1 M phosphatbuffer (0,2 M NaH2PO4 x H2O, 0,2 M NaH2PO4 x 2H2O, 0,1 M CaCl2). Efterfølgende blev nyrerne fjernet, skåret i stykker og frosset i flydende propan og opbevaret ved -80 grader.
Studier af metaboliske bureEfter tilpasning til metaboliske bure (Techniplast) blev mus holdt i metaboliske bure i fire på hinanden følgende dage med fri adgang til postevand og standard laboratoriefoder (Ssniff, Spezialdiäten GmbH). Kropsvægt, mad- og vandindtag blev registreret dagligt, og 24 timers urin og fæces blev opsamlet.
VandbegrænsningsprotokolMus blev holdt i 24 timer i metaboliske bure (Techniplast) uden adgang til postevand. Standard laboratoriefoderpulver (Ssniff, Spezialdiäten GmbH) blev blandet med vand 1:1, 24 timers urin og fæces blev opsamlet og analyseret. Efter 24 timer blev musene sat tilbage i normale bure (T 2L (IVC), LASC, UZH).
Biokemiske målingerUrinkoncentrationer af Na plus, K plus, Ca 2 plus blev analyseret ved flammefotometri (EFOX 5053, Eppendorf). Urin- og plasmakoncentrationer af Mg 2 plus blev målt på Zürich Center for Integrative Rodent Physiology med et SYNCHRON LX ® System(er), UniCel ® DxC 800 Synchron ® Clinical System og Synchron ® System Multi Calibrator. Urinkreatinin blev målt efter Jaffe-metoden. Blodgas- og ionkoncentrationer blev målt i hepariniseret fuldblod ved hjælp af ABL825Flex Blood Gas Analyzer (Radiometer) umiddelbart efter blodopsamling fra vena cava. Plasmaaldosteronniveauer og urinkoncentration af uromodulin (UMOD) blev målt med kommercielt tilgængelige ELISA-kits (Aldosterone ELISA-kit fra Cayman; #501090 og Mouse Uromodulin ELISA-kit fra Abcam; ab245726 henholdsvis).
Kvantitativ polymerasekædereaktion i realtid (RT-qPCR)
RNA blev isoleret fra nyrer og distal colon under anvendelse af SV total RNA isolation kit (PROMEGA). Lige koncentrationer af isoleret RNA (250 ng i 129Sv vs C57BL/6 eller 500 ng i f/f, Δ/Δ og f/Δ) blev omvendt transskriberet til cDNA'er med GoScript™ Reverse Transcriptase-kittet (PROMEGA). De genererede cDNA'er blev yderligere fortyndet med DNAse/RNAse-frit vand (1:5). Primere blev designet til kvantificering af total Slc12a1, Slc12a3, Trpm6, Trpv5, Scnn1a, Scnn1b, Scnn1g og Kcnj1 (tabel S3). Kvantitativ PCR-analyse blev udført under anvendelse af LightCycler® 480 (Roche) for at måle ekspressionsniveauer af generne af interesse. Relativ genekspression blev beregnet under anvendelse af delta Ct-metoden under anvendelse af -actin som referencegenet.

Western blot analyseNyrerne blev homogeniseret i en detergentfri lysisbuffer (DFLB) indeholdende mannitol 200 mM, HEPES [4- (2- hydroxylethyl)- 1piperazinethansulfonsyre syrer] 80 mM, kaliumhydroxid 41 mM, proteasehæmmere (Complete Ultra, Roche) og phosphatasehæmmere (PhosSTOP, Roche) ved anvendelse af 32 Magna Lyser Green Beads (Roche) i en Precellys 24 vævshomogenisator (Bertin Instruments, Montignyle- Bretonneux). Perler blev sedimenteret ved centrifugering i 10 minutter (1987 rcf), og den proteinholdige supernatant blev opbevaret i portioner til engangsbrug ved -80 grader. Til Western blot blev 50 µg protein denatureret i Laemmli Buffer, adskilt ved SDS-PAGE under anvendelse af 8 procent - 12 procent geler og efterfølgende overført til nitrocellulosemembraner. Ikke-specifikke bindingssteder blev blokeret ved hjælp af 1x Odyssey Blocking Solution (Li-COR Biosciences), før membraner blev inkuberet med primære antistoffer (tabel S4) fortyndet i 0,2x Odyssey Blocking Solution ved 4 grader i 12 timer. Efter vask i PBS- 0.1 procent Tween blev membranerne inkuberet med sekundære antistoffer (ged-anti-kanin IRDye 800 eller gede-anti-mus IR farvestof 680, 1:10'000, LI - COR Biosciences) fortyndet i 0,1x kaseinblokerende buffer (Sigma). Detekterede bånd blev visualiseret med Odyssey infrarøde billeddannelsessystem (Li-COR Biosciences). For at sikre ensartet proteinbelastning blev membraner enten co-farvet med et antistof mod - actin eller totalt protein blev farvet ved hjælp af REVERT Total Protein Stain (Li-COR Biosciences) før antistofdetektion. Immunoreaktive bånd blev kvantificeret i Fiji (ImageJ) og normaliseret mod henholdsvis - actin signal eller REVERT Total proteinfarvning.
ImmunhistokemiKryostatsektioner (tykkelse 4 µm) blev blokeret for uspecifik antistofbinding med 10 procent normalt gedeserum og efterfølgende inkuberet med primære antistoffer (tabel S4)
natten over ved 4 grader. Efter vask med 1X PBS blev objektglassene inkuberet med sekundære antistoffer (Cy3 – konjugeret ged-anti-kanin IgG, produktnummer 111- 165- 144, 1:1000 og FITC – konjugeret ged-anti-mus IgG , produktnummer 115- 095- 068, henholdsvis 1:100, begge fra Jackson Immuno Research Laboratories) i 2 timer ved stuetemperatur. Alle antistoffer blev fortyndet i 1 procent BSA/1xPBS. Cellekerner blev farvet med DAPI (4',6- Diamidino- 2-phentyl-indol, Sigma-Aldrich, Co.) i en koncentration på 0,1 µg/ml. Billeddannelse blev udført ved hjælp af et Leica DM6000 B fluorescensmikroskop (Leica Microsystems, 35578) med et Leica DFC350 FX fluorescens monokromt digitalkamera (Leica Microsystems, 35578). Billeder blev behandlet i Fiji (ImageJ).
Generering af affinitetsoprenset kanin-anti-mus pT96 NKCC2 antistofAntistofproduktion blev udført af Pineda antistofservice (Berlin, Tyskland). Kaniner blev immuniseret med et phosphopeptid omfattende aminosyrerne 105- 114 af C57BL/6 muse-NKCC2-sekvensen (NH2- YYLQ(p) TMDAV-COOH). Monospecifik IgG-fraktion blev affinitetsoprenset mod phospho-peptidet og efterfølgende præabsorberet med dephospho-peptidet, hvilket resulterede i en phosphoform-specifik antistoffraktion. Antistofspecificitet af denne fraktion blev testet ved immunhistokemi og Western blot-analyse (figur 5 og figur S4).
Fosfatase behandlingProteinlysater blev inkuberet i 1 time ved 37 grader med kalve intestinal alkalisk phosphatase (CIAP) (1 U/1 µg protein) for at inducere hydrolysen af 5'-phosphatgrupper af phosphoryleret proteiner, hvilket hæmmede den specifikke binding af pT96 NKCC2-antistof mod proteinerne på nitrocellulose Western blot-membran (figur 5B). Arkiverede paraffinindlejrede nyrer fra C57BL6-mus blev anvendt. Behandling af sektioner ved hjælp af kalvetarm alkalisk fosfatase (Sigma Aldrich) blev udført som beskrevet tidligere med mindre modifikationer. 56 Efter blokering af frie aldehydgrupper blev sektioner skyllet fem gange i alkalisk phosphatasebuffer (100 mm Tris, 50 µm CaCl 2, 0,1 mm MgCl 2, 8,4 µm leupeptin, 4 mm Pefablock, pH 9,0). Senere blev sektionerne inkuberet i alkalisk phosphatasebuffer med eller uden kalvetarm alkalisk phosphatase (~130 enheder/ml) i en inkubator ved 35 grader i 2 timer. Immunhistokemi og lysmikroskopi blev efterfølgende udført som detaljeret. 57
AminosyresekvensjusteringAminosyresekvenserne for forskellige arter og musestammer blev opnået fra den åbne database "Ensembl Genome Browser" (www.ensem bl.org, Sanger Institute). 42 Kilderne til transskriptions-id'erne er angivet i tabel S1. Sekvenserne blev justeret ved hjælp af Qiagen © CLC Main Workbench 20.
Nyre skiverNyreskiver af C57BL/6 mus blev brugt til ex vivo eksperimenter som beskrevet tidligere. 12 Kort fortalt blev mus fastet natten over med fri adgang til vand for at undgå eventuelle potentielle virkninger af ionindtagelse i kosten på phosphoryleringsniveauer af NKCC2 og NCC. Nyrerne blev fjernet fra bedøvede dyr, skåret i 280 µm tykke skiver under anvendelse af en vibrerende mikroskærer (Vibratome, Microm; Thermo Scientific) og anbragt i en Ringers opløsning (i mM): 98,5 NaCl, 25 NaHC03, 3 KCl, 1 Na2 HPO 4 , 2,5 CaCl 2 , 1,8 MgCl 2 og 25 glucose i 30 minutter ved 30,5 grader med konstant bobling med 95 procent O 2 og 5 procent CO 2 . Efterfølgende blev Ringer-opløsningen erstattet af lignende opløsninger, men med forskellige Cl − (5 mM for lav Cl − , 110 mM for normal Cl − ) og K plus koncentrationer (3 mM for normal K plus , 10 mM for høj K plus ) for yderligere 30 minutter. Til sidst blev skiverne lynfrosset i flydende nitrogen.
StatistikkerIkke-parret Students t-test og Welchs test i tilfælde af ulige varianser blev brugt til at sammenligne to grupper (GraphPad Prism, Version 8.0.2). Til multipel sammenligning blev en- eller tovejs ANOVA efterfulgt af Tukeys multiple sammenligning post-test udført (GraphPad Prism, Version 8.0.2). Data vises som middel ± SEM (i tabeller og figurer). Forskelle blev anset for at være signifikante, når P <>

ANKENDELSER Forfatterne takker Dr. Gary Shull (University of Cincinnati, Cincinnait, OH) for at levere NCC-KO-musene, Dr. Biff Forbush (Yale School of Medicine, New Haven, CT) for hans "R5" pNKCC1-antistof, og Dr. Henrik Dimke ( Syddansk Universitet, Odense, Danmark) for sit muse monoklonale totale NCC-antistof. Forfatterne anerkender også Monique Carrell og Inger Merete Paulsen for teknisk assistance og Dr. Eszter Banki for at ydenyreprøver. Knoglemineraldensitetsmålingerne og en del af urin- og plasmaanalysen blev udført af henholdsvis Dr. Petra Seebeck og Nadine Nägele (Zurich Integrative Rodent Physiology, University of Zurich). Meget værdsat var det meget nyttige input fra Dr. Alicia McDonough (University of Southern California) og Dr. Olivier Devuyst (University of Zurich).
INTERESSEKONFLIKT Gruppen af JL modtager royalties for licenserede antistoffer mod NCC og phosphoryleret Nedd4- 2 fra henholdsvis Milipore og Abcam. Begge antistoffer blev ikke brugt i den aktuelle undersøgelse. JL modtog desuden i 2019 et honorar fra VIFOR for en mundtlig præsentation ved et symposium arrangeret af VIFOR.
